Phần 1. Hóa học
Phần 2. Vật lý
- Bài 7: Các đại lượng cơ bản của dòng điện một chiều trong đoạn mạch
- Bài 8: Định luật Ôm, xác định điện trở dây dẫn bằng ampe kế và vôn kế
- Bài 9: Đoạn mạch nối tiếp và đoạn mạch song song
- Bài 10: Các yếu tố ảnh hưởng tới điện trở
- Bài 11: Điện năng, công, công suất điện
- Bài 12: Sử dụng an toàn và tiết kiệm điện
- Bài 13: Tổng kết phần dòng điện một chiều
Phần 3. Sinh học
- Bài 14: Giới thiệu về di truyền học
- Bài 15: Nhiễm sắc thể
- Bài 16: Chu kì tế bào và nguyên phân
- Bài 17: Giảm phân và thụ tinh
- Bài 18: Nhiễm sắc thể giới tính và cơ chế xác định giới tính
- Bài 19: ADN và gen
- Bài 20: ARN, mối quan hệ giữa gen và ARN
- Bài 21: Mối quan hệ giữa gen và tính trạng
- Bài 22: Đột biến gen
- Bài 23: Đột biến cấu trúc nhiễm sắc thể
- Bài 24: Đột biến số lượng nhiễm sắc thể
- Bài 25: Di truyền học Menđen - Lai một cặp tính trạng
- Bài 26: Di truyền học Menđen - Lai hai cặp tính trạng
- Bài 27: Di truyền liên kết và liên kết với giới tính
- Bài 28: Mối quan hệ giữa kiểu gen - Môi trường - Kiểu hình
- Bài 29: Di truyền học người
- Bài 30: Di truyền y học tư vấn
- Bài 31: Ôn tập phần Di truyền và biến dị
Phần 1: Hóa học
- Bài 32: Đại cương về hóa học hữu cơ
- Bài 33: Metan
- Bài 34: Etilen - Axetilen
- Bài 35: Benzen
- Bài 36: Dầu mỏ và khí thiên nhiên - Nhiên liệu
- Bài 37: Ôn tập chủ để 8: Hidrocacbon - Nhiên liệu
- Bài 38: Rượu etylic
- Bài 39: Axit axetic
- Bài 40: Mối liên hệ giữa etylen, rượu etylic và axit axetic
- Bài 41: Chất béo
- Bài 42: Cacbonhidrat
- Bài 43: Protein
- Bài 44: Polime
- Bài 45: Ôn tập chủ để 9: Dẫn xuất của hidrocacbon - polime
Phần 2: Vật lí
- Bài 46: Từ trường
- Bài 47: Nam châm điện
- Bài 48: Lực điện từ - Động cơ điện một chiều
- Bài 49: Hiện tượng cảm ứng điện từ
- Bài 50: Dòng điện xoay chiều
- Bài 51: Truyền tải điện năng - Máy biến áp
- Bài 52: Tổng kết phần điện từ học
- Bài 53: Ảnh của một vật tạo bởi gương
- Bài 54: Ảnh của một vật tạo bởi thấu kính
- Bài 55: Máy ảnh, mắt và kính lúp
- Bài 56: Các tác dụng của ánh sáng
- Bài 57: Tổng kết phần quang học
- Bài 57: Tổng kết phần quang học
- Bài 58: Chuyển hóa năng lượng. Định luật bảo toàn và chuyển hóa năng lượng
- Bài 59: Ôn tập phần vật lí
Phần 3: Sinh học
- Bài 60: Lai giống vật nuôi, cây trồng
- Bài 61: Công nghệ tế bào
- Bài 62: Công nghệ gen
- Bài 64: Ôn tập chủ đề 13. Ứng dụng Di truyền học
- Bài 65: Sinh vật thích nghi kì diệu với môi trường
- Bài 66: Luyện tập sinh vật với môi trường
- Bài 67: Ôn tập chủ đề 14. Sinh vật với môi trường
- Bài 68: Tổng kết chương trình sinh học toàn cấp trung học cơ sở
Bài 6: Ôn tập hóa học vô cơ
https://s.shopee.vn/2LVIrhIyVS
Bài 6: Ôn tập hóa học vô cơ - sách VNEN khoa học tự nhiên 9 tập 1
Trong bài học này, chúng ta sẽ cùng nhau ôn tập kiến thức về hóa học vô cơ. Bài học nằm trong sách VNEN khoa học tự nhiên 9 tập 1 bài 6 trang 31. Chúng ta sẽ quay lại các kiến thức đã học và giải đáp các câu hỏi được đề cập trong bài. Cách làm chi tiết và dễ hiểu sẽ được hướng dẫn để giúp các em học sinh nắm vững kiến thức.
Bài học này nhằm mục đích giúp học sinh ôn tập và củng cố kiến thức về hóa học vô cơ, từ đó nắm vững căn bản để áp dụng vào các bài tập và bài kiểm tra. Hy vọng rằng bài học sẽ giúp các em hiểu rõ và tự tin hơn trong việc học tập và áp dụng kiến thức này vào cuộc sống hàng ngày.
Bài tập và hướng dẫn giải
1. Viết PTHH của các phản ứng (nếu có) trong các các trường hợp sau:
a, $H_{2} + Fe_{2}O_{3} \overset{t^{o}}{\rightarrow} $
b, $H_{2} + Al_{2}O_{3} \overset{t^{o}}{\rightarrow} $
c, $Ca + H_{2}O \rightarrow $
d, $Mg + H_{2}O \rightarrow$
e, $K_{2}O + H_{2}O \rightarrow $
2. a, Viết PTHH biểu diễn sự chuyển hóa sau đây:
$S\overset{(1)}{\rightarrow} H_{2}S \overset{(2)}{\rightarrow} Na_{2}S \overset{(3)}{\rightarrow} PbS$
b, Viết PTHH của các phản ứng (nếu có) trong các trường hợp sau:
1) $CO + Fe_{2}O_{3} \overset{t^{o}}{\rightarrow} $
2) $CO + MgO \overset{t^{o}}{\rightarrow}$
3) $C + PbO \overset{t^{o}}{\rightarrow} $
4) $ Cl_{2} + H_{2}O \rightleftharpoons $
5) $Cl_{2} + NaOH \rightarrow $
6) $Br_{2} + NaI\rightarrow r$
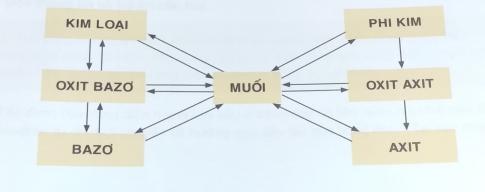
3. Viết PTHH (lấy ví dụ với các chất cụ thể) theo dãy chuyển hóa sau:
4. a, Em hãy cho biết vị trí của nguyên tố lưu huỳnh trong bảng tuần hoàn các nguyên tố hóa học (ô nguyên tố, chu kì, nhóm).
b, Cho biết tính chất hóa học của lưu huỳnh và so sánh với tính chất hóa học của các nguyên tố: O, P, Se. Giải tích.
5. Ngâm một lá sắt trong 100 ml dung dịch CuSO4. Sau khi kết thúc phản ứng, lấy lá sắt ra rửa nhẹ, làm khô rồi đem cân, thấy khối lượng lá sắt tăng thêm 0,2 gam so với khối lượng lá sắt ban đầu (giả thiết toàn bộ lượng đồng bám trên lá săt). Xác định nồng độ mol của dung dịch CuSO4 đã dùng.
6.Hỗn hợp A ở dạng bột gồm Al và Fe. Trộn đều hỗn hợp A rồi chia làm 2 phần bằng nhau.
Cho phần 1 tác dụng với H2SO4 loãng dư thu được 0,784 l khí H2.
Cho phần 2 tác dụng với NaOH dư thu được 0,336 l khí H2
(Biết các phản ứng xảy ra hoàn toàn, các thể tích khí được đo ở đktc). Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp A nói trên.
7. Từ một tấn quặng hematit chứa 58% Fe2O3 có thể sản xuất được bao nhiêu tấn gang chứa 95,5% sắt. Biết hiệu suất của quá trình sản xuất là 85%.
Giải bài tập sách giáo khoa (SGK) lớp 9
- Soạn văn lớp 9 tập 1
- Soạn văn lớp 9 tập 2
- Soạn văn lớp 9 tập 1 giản lược
- Soạn văn lớp 9 tập 2 giản lược
- Giải bài tập sách giáo khoa (SGK) toán lớp 9 tập 1
- Giải bài tập sách giáo khoa (SGK) toán lớp 9 tập 2
- Giải bài tập sách giáo khoa (SGK) sinh học lớp 9
- Giải bài tập sách giáo khoa (SGK) hoá học lớp 9
- Giải bài tập sách giáo khoa (SGK) vật lí lớp 9
- Giải bài tập sách giáo khoa (SGK) địa lí lớp 9
- Giải bài tập sách giáo khoa (SGK) lịch sử lớp 9
- Giải bài tập sách giáo khoa (SGK) gdcd lớp 9
- Giải bài tập sách giáo khoa (SGK) tiếng anh lớp 9
- Giải bài tập mĩ thuật lớp 9 Đan Mạch
Giải bài tập sách giáo khoa (SGK) lớp 9 VNEN
- Soạn văn lớp 9 tập 1 VNEN
- Soạn văn lớp 9 tập 2 VNEN
- Soạn văn lớp 9 VNEN siêu ngắn
- Soạn văn lớp 9 VNEN tập 1 giản lược
- Soạn văn lớp 9 VNEN tập 2 giản lược
- Giải bài tập toán lớp 9 tập 1 VNEN
- Giải bài tập toán lớp 9 tâp 2 VNEN
- Giải bài tập khoa học tự nhiên lớp 9
- Giải bài tập khoa học xã hội lớp 9
- Giải bài tập gdcd lớp 9 VNEN
- Giải bài tập công nghệ lớp 9 VNEN
- Giải bài tập tin học lớp 9 VNEN
- Giải bài tập tiếng anh lớp 9 mới - Tập 1
- Giải bài tập tiếng anh lớp 9 mới - Tập 2
Tài liệu lớp 9
- Văn mẫu lớp 9
- Đề thi lên 10 Toán
- Đề thi môn Hóa lớp 9
- Đề thi môn Địa lớp 9
- Đề thi môn vật lí lớp 9
- Tập bản đồ địa lí lớp 9
- Ôn toán lớp 9 lên 10
- Ôn Ngữ văn lớp 9 lên 10
- Ôn tiếng anh lớp 9 lên 10
- Đề thi lên 10 chuyên Toán
- Chuyên đề ôn tập Hóa lớp 9
- Chuyên đề ôn tập Sử lớp 9
- Chuyên đề toán lớp 9
- Chuyên đề Địa Lý lớp 9
- Phát triển năng lực toán lớp 9 tập 1
- Bài tập phát triển năng lực toán lớp 9




