CHƯƠNG 1: CẤU TẠO NGUYÊN TỬ
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 2 Thành phần của nguyên tử
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 3 Nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 4 Cấu trúc lớp vỏ electron của nguyên tử
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo Ôn tập chương 1
CHƯƠNG 2: BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 5 Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 6 Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kì và nhóm
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 7 Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo Ôn tập chương 2
CHƯƠNG 3: LIÊN KẾT HÓA HỌC
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 8 Quy tắc Octet
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 9 Liên kết ion
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 10 Liên kết cộng hóa trị
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 11 Liên kết Hydrogen và tương tác Van Der Waals
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài Ôn tập chương 3
CHƯƠNG 4: PHẢN ỨNG OXI HÓA-KHỬ
CHƯƠNG 5: NĂNG LƯỢNG HÓA HỌC
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 13 Enthalpy tạo thành và biến thiên Emthalpy của phản ứng hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 14 Tính biến thiên của enthalpy của phản ứng hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài Ôn tập chương 5
CHƯƠNG 6: TỐC ĐỘ PHẢN ỨNG HÓA HỌC
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 15 Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 16 Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài Ôn tập chương 6
CHƯƠNG 7: NGUYÊN TỐ NHÓM VIIA- HALOGEN
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 17 Tính chất vật lí và hóa học các đơn chất nhóm
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 18 Hydrogen Halide và một số phản ứng của ion Halide
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo Ôn tập chương 7
Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài Ôn tập chương 4
https://s.shopee.vn/AKN2JyAJAw
Hướng dẫn giải bài Ôn tập chương 4 trang 49 sách bài tập (SBT) Hoá học 10
Trong bộ sách bài tập "Chân trời sáng tạo", chương 4 là một phần quan trọng giúp học sinh nắm vững kiến thức về Hoá học 10. Trang 49 sách bài tập (SBT) là bài ôn tập nhằm giúp học sinh củng cố kiến thức, chuẩn bị cho các bài kiểm tra, thi cử.
Để giải bài Ôn tập chương 4 trang 49, học sinh cần chú ý đến từng bước giải bài một cách cụ thể. Việc hướng dẫn chi tiết và giải đáp thắc mắc giúp học sinh hiểu sâu về bài học, từ đó nắm vững kiến thức và áp dụng linh hoạt vào thực hành.
Với sự hướng dẫn cụ thể, dễ hiểu và đầy sắc thái, sách bài tập (SBT) Hoá học 10 giúp học sinh phát triển kỹ năng giải toán, tư duy logic và xây dựng nền tảng kiến thức vững chắc trong môn Hoá học.
Bài tập và hướng dẫn giải
OT4.1. Sản xuất gang trong công nghiệp bằng cách sử dụng khí CO khử Fe2O3 ở nhiệt độ cao theo phản ứng sau:
Fe2O3+ 3CO $\overset{t^{o}}{\rightarrow}$ 2Fe + 3CO2
Trong phản ứng trên chất đóng vai trò chất khử là
A. Fe2O3. B. CO. C. Fe. D. CO2
OT4.2. Cho các phân tử có công thức cấu tạo sau:
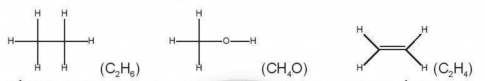
Số oxi hoá trung bình của nguyên tử C trong các phân tử trên lần lượt là
A. -3, -2, -2. B. -3, -3, -2. C. - 2, -2, -2. D. -3, -2, -3.
OT4.3. Thực hiện các phản ứng sau:
(a) Ca(OH)2 + Cl2 →CaOCI2 + H2O
(b) 3Cl2 + 6KOH $\overset{t^{o}}{\rightarrow}$ 5KCI + KCIO3 + 3H2O
(c) Cl2 + 2FeCl2 → 2FeCl3
(d) 2KCIO3 $\overset{t^{o}}{\rightarrow}$ 2KCI + 3O2
Số phản ứng chlorine đóng vai trò chất oxi hoá là
A. 1. B. 2. C. 3. D. 4.
OT4.4. Bromine vừa là chất oxi hoá, vừa là chất khử trong phản ứng nào sau đây?
A. 3Br2 + 6NaOH → 5NaBr + NaBrO3 + 3H2O.
B. Br2 + H2 $\overset{t^{o}}{\rightarrow}$ 2HBr.
C. 3Br2 + 2Al→ 2AlBr3.
D. Br2 + 2KI → I2+ 2KBr.
OT4.5. Nguyên tử sulfur chỉ thể hiện tính khử (trong điều kiện phản ứng phù hợp) trong hợp chất nào sau đây?
A. SO2 B. H2SO4 C. H2S. D. Na2SO3.
OT4.6. Tính số oxi hoá các nguyên tố có đánh dấu *:

OT4.7. Chất được gạch chân trong các phương trình hoá học sau đây là chất oxi hoá hay chất khử, nêu lí do.
a) Br2+ 2KI → I2 + 2KBr
b) 3Zn + 8HNO3 → 3Zn(NO3)2 + 3NO + 4H2O
c) K2Cr2O7 + 14HCI → 2CrCl3 + 2KCI + 3Cl2 + 7H2O
OT4.8. Dẫn ra hai phản ứng, trong đó có một phản ứng oxi hoá – khử và một không phải phản ứng oxi hoá khử.
OT4.9. Dưới tác dụng của các chất xúc tác, glucose tạo thành các sản phẩm khác nhau.
– Lên men tạo thành ethanol
C6H12O6 (glucose) $\overset{enzyme }{\rightarrow}$ C2H5OH(ethanol) + CO2 (1)
– Ethanol lên men thành acetic acid:
CH3 - CH2 - OH + O2 $\overset{enzyme }{\rightarrow}$ CH3 - COOH (acetic acid) + H2O (2)
a) Cho biết vai trò của các chất trong các phản ứng (1) và (2).
b) Tính lượng glucose cần dùng để thu được 1 lit acetic acid 1 M. Giả sử hiệu suất của cả quá trình là 50%.
OT4.10. Ion Ca2+ cần thiết cho máu của người hoạt động bình thường. Nồng độ ion calcium không bình thường là dấu hiệu của bệnh. Để xác định nồng độ ion calcium, người ta lấy mẫu máu, sau đó kết tủa ion calcium dưới dạng calcium oxalate (CaC2O4) rồi cho calcium oxalate tác dụng với dung dịch potassium permanganate trong môi trường acid theo phản ứng sau: CaC2O4 + KMnO4 + H2SO4 → CaSO4 + K2SO4 + MnSO4 + H2O + CO2
a) Cân bằng phương trình phản ứng. trình phản ứng
b) Giả sử calcium oxalate kết tủa từ 1 mL máu một người tác dụng vừa hết với 2,05 mL dung dịch potassium permanganate (KMnO4)4,88.10-4M. Xác định nồng độ ion calcium trong máu người đó bằng đơn vị mg Ca2+/100 mL máu.
OT4.11. Hỗn hợp ammonium perchlorate (NH4CIO4) và bột nhôm là nhiên liệu rắn của tàu vũ trụ con thoi theo phản ứng sau: NH4CIO4 → N2↑ + Cl2↑ + O2↑+ H2O
Mỗi một lần phóng tàu con thoi tiêu tốn 750 tấn ammonium perchlorate. Giả sử tất cả oxygen sinh ra tác dụng với bột nhôm, hãy tính khối lượng nhôm phản ứng với oxygen và khối lượng aluminium oxide sinh ra.
OT4.12. Cho 30,3g hỗn hợp Al và Zn tác dụng vừa đủ với 11,15 lít O2 (đkc) thu được hỗn hợp các oxide. Viết các phương trình hóa học xảy ra và tính khối lượng các oxide tạo thành.
OT4.13. Sodium peroxide (Na2O2), potassium superoxide (KO2) là những chất oxi hoá mạnh, dễ dàng hấp thụ khi carbon dioxide và giải phóng khí oxygen. Do đó, chúng được sử dụng trong binh lặn hoặc tàu ngầm để hấp thụ khí carbon dioxide và cung cấp khí oxygen cho con người trong hô hấp theo các phản ứng sau:
Na2O2 + CO2 → Na2CO3+ O2↑
KO2 + CO2→ K2CO3 + O2↑
a) Cân bằng các phản ứng biết rằng nguyên tử oxygen trong Na2O2, KO2 là nguyên tố tự oxi hoá – khử.
b) Theo nghiên cứu, khi hô hấp, thể tích khí carbon dioxide một người thải ra xấp xỉ thể tích khí oxygen hít vào. Cần trộn Na2O2, KO2 theo tỉ lệ số mol như thế nào để thể tích khí carbon dioxide hấp thụ bằng thể tích khí oxygen sinh ra?
OT4.14. Copper (II) sulfate được sử dụng làm nguyên liệu trong phân bón, làm thuốc kháng nấm. Ngoài ra, còn dùng để diệt rêu – tảo trong bể bơi,... Copper (II) sulfate được sản xuất chủ yếu sử dụng từ nguồn nguyên liệu tái chế. Phế liệu được tinh chế cùng kim loại nóng chảy được đổ vào nước để tạo thành những mảnh xốp. Hỗn hợp này được hoà tan trong dung dịch sulfuric acid loãng trong không khí theo phương trình:
Cu + O2 + H2SO4 → CuSO4 + H2O (1).
Ngoài ra, copper (II) sulfate còn được điều chế bằng cách cho đồng phế liệu tác dụng với dung dịch sunfuric acid đặc, nóng:
Cu + H2SO4 → CuSO4 + SO2 + H2O (2).
a) Cân bằng 2 phản ứng trên theo phương pháp thăng bằng electron.
b) Trong hai cách trên, cách nào ít làm ô nhiễm môi trường hơn?
OT4.15. Cho 1,12 g kim loại X tác dụng với dung dịch sulfuric acid đặc, nóng, dư thu được 0,7437 lít khí SO2 (đkc) và muối X2(SO4)3.
a) Viết phản ứng và cân bằng phương trình hoá học theo phương pháp thăng bằng electron.
b) Xác định kim loại X.
Giải bài tập sách giáo khoa (SGK) 10 Kết nối tri thức
- Soạn văn lớp 10 tập 1 kết nối tri thức
- Soạn văn lớp 10 tập 2 kết nối tri thức
- Văn mẫu lớp 10 kết nối tri thức
- Giải bài tập toán lớp 10 tập 1 kết nối tri thức
- Giải bài tập toán lớp 10 tập 2 kết nối tri thức
- Giải bài tập vật lí lớp 10 kết nối tri thức
- Giải bài tập hóa học lớp 10 kết nối tri thức
- Giải bài tập sinh học lớp 10 kết nối tri thức
- Giải bài tập Địa lí lớp 10 kết nối tri thức
- Giải bài tập lịch sử lớp 10 kết nối tri thức
- Giải bài tập tin học lớp 10 kết nối tri thức
- Giải bài tập Âm nhạc lớp 10 kết nối tri thức
- Giải bài tập mĩ thuật lớp 10 kết nối tri thức
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 kết nối tri thức
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 kết nối tri thức
- Giải bài tập hoạt động trải nghiệm lớp 10 kết nối tri thức
- Giải bài tập thiết kế công nghệ lớp 10 kết nối tri thức
- Giải bài tập công nghệ trồng trọt lớp 10 kết nối tri thức
- Giải bài tập giáo dục thể chất lớp 10 kết nối tri thức
- Giải bài tập tiếng anh lớp 10 Global Success
Giải bài tập sách giáo khoa (SGK) 10 Chân trời sáng tạo
- Soạn văn lớp 10 tập 1 chân trời sáng tạo
- Soạn văn lớp 10 tập 2 chân trời sáng tạo
- Văn mẫu lớp 10 chân trời sáng tạo
- Giải bài tập toán lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập toán lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập vật lí lớp 10 chân trời sáng tạo
- Giải bài tập hóa học lớp 10 chân trời sáng tạo
- Giải bài tập sinh học lớp 10 chân trời sáng tạo
- Giải bài tập Địa lí lớp 10 chân trời sáng tạo
- Giải bài tập lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập tin học lớp 10 chân trời sáng tạo
- Giải bài tập Âm nhạc lớp 10 chân trời sáng tạo
- Giải bài tập mĩ thuật lớp 10 chân trời sáng tạo
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập Hoạt động trải nghiệm, hướng nghiệp lớp 10 chân trời sáng tạo bản 1
- Giải bài tập Hoạt động trải nghiệm, hướng nghiệp lớp 10 chân trời sáng tạo bản 2
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 chân trời sáng tạo
- Giải bài tập thiết kế công nghệ lớp 10 chân trời sáng tạo
- Giải bài tập công nghệ trồng trọt lớp 10 chân trời sáng tạo
- Giải bài tập giáo dục thể chất lớp 10 chân trời sáng tạo
- Giải bài tập tiếng anh lớp 10 Friends Global
Giải bài tập sách giáo khoa (SGK) 10 Cánh diều
- Soạn văn lớp 10 tập 1 cánh diều
- Soạn văn lớp 10 tập 2 cánh diều
- Văn mẫu lớp 10 cánh diều
- Giải bài tập toán lớp 10 tập 1 cánh diều
- Giải bài tập toán lớp 10 tập 2 cánh diều
- Giải bài tập vật lí lớp 10 cánh diều
- Giải bài tập hóa học lớp 10 cánh diều
- Giải bài tập sinh học lớp 10 cánh diều
- Giải bài tập Địa lí lớp 10 cánh diều
- Giải bài tập lịch sử lớp 10 cánh diều
- Giải bài tập tin học lớp 10 cánh diều
- Giải bài tập Âm nhạc lớp 10 cánh diều
- Giải bài tập mĩ thuật lớp 10 cánh diều
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 cánh diều
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 cánh diều
- Giải bài tập hoạt động trải nghiệm lớp 10 cánh diều
- Giải bài tập thiết kế công nghệ lớp 10 cánh diều
- Giải bài tập công nghệ trồng trọt lớp 10 cánh diều
- Giải bài tập giáo dục thể chất lớp 10 cánh diều
- Giải bài tập tiếng anh lớp 10 Explore new worlds
Giải bài tập sách bài tập (SBT) lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tin học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Global success
Giải bài tập sách bài tập (SBT) lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 chân trời sáng tạo bản 1
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 chân trời sáng tạo bản 2
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Friends Global
Giải bài tập sách bài tập (SBT) lớp 10 Cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) tin học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Explore new world
Giải bài tập chuyên đề học tập 10 Kết nối tri thức
- Giải bài tập chuyên đề toán lớp 10 kết nối tri thức
- Giải bài tập chuyên đề ngữ văn lớp 10 kết nối tri thức
- Giải bài tập chuyên đề vật lí lớp 10 kết nối tri thức
- Giải bài tập chuyên đề hóa học lớp 10 kết nối tri thức
- Giải bài tập chuyên đề sinh học lớp 10 kết nối tri thức
- Giải bài tập chuyên đề lịch sử lớp 10 kết nối tri thức
- Giải bài tập chuyên đề địa lí lớp 10 kết nối tri thức
- Giải bài tập chuyên đề công nghệ trồng trọt lớp 10 kết nối tri thức
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng tin học ứng dụng kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng khoa học máy tính kết nối tri thức
- Giải bài tập chuyên đề mĩ thuật lớp 10 kết nối tri thức
Giải bài tập chuyên đề học tập 10 Chân trời sáng tạo
- Giải bài tập chuyên đề toán lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề ngữ văn lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề vật lí lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề hóa học lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề sinh học lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề địa lí lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề âm nhạc lớp 10 chân trời sáng tạo
Giải bài tập chuyên đề học tập 10 Cánh diều
- Giải bài tập chuyên đề toán lớp 10 cánh diều
- Giải bài tập chuyên đề ngữ văn lớp 10 cánh diều
- Giải bài tập chuyên đề vật lí lớp 10 cánh diều
- Giải bài tập chuyên đề hóa học lớp 10 cánh diều
- Giải bài tập chuyên đề sinh học lớp 10 cánh diều
- Giải bài tập chuyên đề địa lí lớp 10 cánh diều
- Giải bài tập chuyên đề lịch sử lớp 10 cánh diều
- Giải bài tập chuyên đề công nghệ trồng trọt lớp 10 cánh diều
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 cánh diều
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng tin học ứng dụng cánh diều
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng khoa học máy tính cánh diều
- Giải bài tập chuyên đề âm nhạc lớp 10 cánh diều




