CHƯƠNG 1: CẤU TẠO NGUYÊN TỬ
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 2 Thành phần của nguyên tử
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 3 Nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 4 Cấu trúc lớp vỏ electron của nguyên tử
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo Ôn tập chương 1
CHƯƠNG 2: BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 5 Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 6 Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kì và nhóm
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 7 Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo Ôn tập chương 2
CHƯƠNG 3: LIÊN KẾT HÓA HỌC
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 8 Quy tắc Octet
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 9 Liên kết ion
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 10 Liên kết cộng hóa trị
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 11 Liên kết Hydrogen và tương tác Van Der Waals
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài Ôn tập chương 3
CHƯƠNG 4: PHẢN ỨNG OXI HÓA-KHỬ
CHƯƠNG 5: NĂNG LƯỢNG HÓA HỌC
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 13 Enthalpy tạo thành và biến thiên Emthalpy của phản ứng hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 14 Tính biến thiên của enthalpy của phản ứng hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài Ôn tập chương 5
CHƯƠNG 6: TỐC ĐỘ PHẢN ỨNG HÓA HỌC
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 15 Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 16 Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài Ôn tập chương 6
CHƯƠNG 7: NGUYÊN TỐ NHÓM VIIA- HALOGEN
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 17 Tính chất vật lí và hóa học các đơn chất nhóm
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài 18 Hydrogen Halide và một số phản ứng của ion Halide
- Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo Ôn tập chương 7
Giải bài tập sách bài tập (SBT) Hoá học 10 chân trời sáng tạo bài Ôn tập chương 6
https://s.shopee.vn/AKN2JyAJAw
Hướng dẫn giải bài Ôn tập chương 6 trang 73 sách bài tập (SBT) Hoá học 10
Bài tập ôn tập chương 6 trong sách bài tập Hoá học 10 là một phần quan trọng giúp học sinh củng cố kiến thức về chương trình hóa học. Hướng dẫn giải chi tiết và cụ thể sẽ giúp học sinh hiểu rõ hơn về nội dung bài học.
Bài tập này được biên soạn theo chương trình đổi mới của Bộ giáo dục, đảm bảo đáp ứng đầy đủ các kiến thức cần thiết. Việc hướng dẫn giải bài tập một cách rõ ràng, dễ hiểu sẽ giúp học sinh tự tin khi làm bài và nắm vững kiến thức.
Hi vọng rằng, thông qua việc giải bài tập ôn tập chương 6 trang 73, học sinh sẽ củng cố và mở rộng kiến thức, chuẩn bị tốt cho kì thi sắp tới.
Bài tập và hướng dẫn giải
OT6.1. Phản ứng 2NO (g) + O2 (g) → 2NO2 (g) có biểu thức tốc độ tức thời:
$v = k.C_{NO}^{2}.C_{O_{2}}$. Nếu nồng độ của NO giảm 2 lần, giữ nguyên nồng độ oxygen, thì tốc độ sẽ
A. giảm 2 lần. B. giảm 4 lần.
C. giảm 3 lần. D. giữ nguyên.
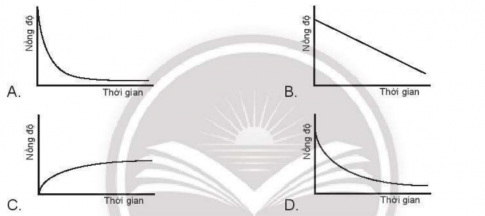
OT6.2. Nếu mỗi đồ thị có các chất phản ứng cùng nồng độ và trục thời gian thì tốc độ của chất phản ứng nào xảy ra nhanh nhất?
OT6.3. Thanh phát sáng là một sản phẩm quen thuộc được dùng giải trí. Đặt 2 thanh phát quang hoá học vào 2 cốc nước nóng (trái) và lạnh (phải) như hình bên, yếu tố ảnh hưởng đến độ phát sáng của 2 thanh là
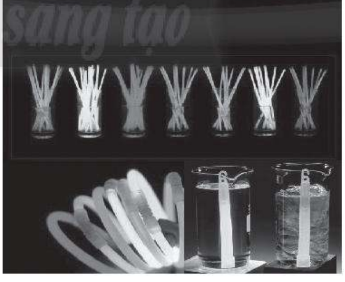
A. nồng độ. B. chất xúc tác.
C. bề mặt tiếp xúc. D. nhiệt độ.
OT6.4. Trong hầu hết các phản ứng hoá học, tốc độ phản ứng tăng khi nhiệt độ tăng. Muốn pha một cốc trà đá có đường, bằng cách thêm đá viên và đường vào cốc trà nóng, thứ tự nào sẽ được cho vào trước?
OT6.5. Cho phương trình hoá học của phản ứng: 2CO (g) + O2 (g) → 2CO2 (g)
Với biểu thức tốc độ tức thời là: $v = k.C_{CO}^{2}.C_{O_{2}}$., khi nồng độ mol của CO là 1 M và O2 là 1 M, tính giá trị v và nêu ý nghĩa của k.
OT6.6. Từ thí nghiệm ảnh hưởng của bề mặt tiếp xúc đến tốc độ phản ứng trong sách giáo khoa (SGK) trang 101, 102, nếu ở bình (2), sau thời gian 60 giây, thể tích khí CO2 thu được là 30 mL. Tính tốc độ trung bình (mL/s) của phản ứng trong 60 giây.
OT6.7. Trong phản ứng: A → sản phẩm
Tại thời điểm t = 0, nồng độ chất A là 0,1563 M, sau 1 phút, nồng độ chất A là 0,1496 M và sau 2 phút, nồng độ chất A là 0,1431 M.
a) Tinh tốc độ trung bình của phản ứng trong phút thứ nhất và trong phút thứ 2.
b) Nhận xét tốc độ phản ứng trong phút thứ nhất và phút thứ 2. Giải thích.
OT6.8. Xét phản ứng phân huỷ N2O5 theo phương trình hoá học: N2O5 (g) → 4NO2 (g) + O2 (g), xảy ra ở 56°C cho kết quả theo bảng:
Thời gian (s) | N2O5 (M) | NO2 (M) | O2 (M) |
240 | 0,0388 | 0,0315 | 0,0079 |
600 | 0,0196 | 0,0699 | 0,0175 |
Tính tốc độ trung bình của phản ứng trong khoảng thời gian trên.
OT6.9. Sự phân huỷ H2O2 theo phương trình hoá học:
2H2O2(aq) → 2H2O (l) + O2 (g),
được nghiên cứu và cho kết quả tại một nhiệt độ cụ thể như sau:
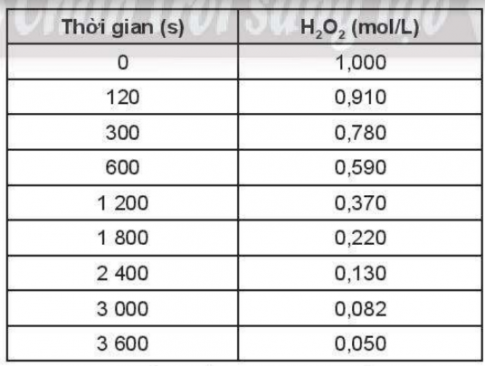
a) Tính tốc độ trung bình của phản ứng phân huỷ H2O2 theo thời gian.
b) Tốc độ phản ứng thay đổi thế nào theo thời gian? Giải thích sự thay đổi đó.
Giải bài tập sách giáo khoa (SGK) 10 Kết nối tri thức
- Soạn văn lớp 10 tập 1 kết nối tri thức
- Soạn văn lớp 10 tập 2 kết nối tri thức
- Văn mẫu lớp 10 kết nối tri thức
- Giải bài tập toán lớp 10 tập 1 kết nối tri thức
- Giải bài tập toán lớp 10 tập 2 kết nối tri thức
- Giải bài tập vật lí lớp 10 kết nối tri thức
- Giải bài tập hóa học lớp 10 kết nối tri thức
- Giải bài tập sinh học lớp 10 kết nối tri thức
- Giải bài tập Địa lí lớp 10 kết nối tri thức
- Giải bài tập lịch sử lớp 10 kết nối tri thức
- Giải bài tập tin học lớp 10 kết nối tri thức
- Giải bài tập Âm nhạc lớp 10 kết nối tri thức
- Giải bài tập mĩ thuật lớp 10 kết nối tri thức
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 kết nối tri thức
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 kết nối tri thức
- Giải bài tập hoạt động trải nghiệm lớp 10 kết nối tri thức
- Giải bài tập thiết kế công nghệ lớp 10 kết nối tri thức
- Giải bài tập công nghệ trồng trọt lớp 10 kết nối tri thức
- Giải bài tập giáo dục thể chất lớp 10 kết nối tri thức
- Giải bài tập tiếng anh lớp 10 Global Success
Giải bài tập sách giáo khoa (SGK) 10 Chân trời sáng tạo
- Soạn văn lớp 10 tập 1 chân trời sáng tạo
- Soạn văn lớp 10 tập 2 chân trời sáng tạo
- Văn mẫu lớp 10 chân trời sáng tạo
- Giải bài tập toán lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập toán lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập vật lí lớp 10 chân trời sáng tạo
- Giải bài tập hóa học lớp 10 chân trời sáng tạo
- Giải bài tập sinh học lớp 10 chân trời sáng tạo
- Giải bài tập Địa lí lớp 10 chân trời sáng tạo
- Giải bài tập lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập tin học lớp 10 chân trời sáng tạo
- Giải bài tập Âm nhạc lớp 10 chân trời sáng tạo
- Giải bài tập mĩ thuật lớp 10 chân trời sáng tạo
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập Hoạt động trải nghiệm, hướng nghiệp lớp 10 chân trời sáng tạo bản 1
- Giải bài tập Hoạt động trải nghiệm, hướng nghiệp lớp 10 chân trời sáng tạo bản 2
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 chân trời sáng tạo
- Giải bài tập thiết kế công nghệ lớp 10 chân trời sáng tạo
- Giải bài tập công nghệ trồng trọt lớp 10 chân trời sáng tạo
- Giải bài tập giáo dục thể chất lớp 10 chân trời sáng tạo
- Giải bài tập tiếng anh lớp 10 Friends Global
Giải bài tập sách giáo khoa (SGK) 10 Cánh diều
- Soạn văn lớp 10 tập 1 cánh diều
- Soạn văn lớp 10 tập 2 cánh diều
- Văn mẫu lớp 10 cánh diều
- Giải bài tập toán lớp 10 tập 1 cánh diều
- Giải bài tập toán lớp 10 tập 2 cánh diều
- Giải bài tập vật lí lớp 10 cánh diều
- Giải bài tập hóa học lớp 10 cánh diều
- Giải bài tập sinh học lớp 10 cánh diều
- Giải bài tập Địa lí lớp 10 cánh diều
- Giải bài tập lịch sử lớp 10 cánh diều
- Giải bài tập tin học lớp 10 cánh diều
- Giải bài tập Âm nhạc lớp 10 cánh diều
- Giải bài tập mĩ thuật lớp 10 cánh diều
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 cánh diều
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 cánh diều
- Giải bài tập hoạt động trải nghiệm lớp 10 cánh diều
- Giải bài tập thiết kế công nghệ lớp 10 cánh diều
- Giải bài tập công nghệ trồng trọt lớp 10 cánh diều
- Giải bài tập giáo dục thể chất lớp 10 cánh diều
- Giải bài tập tiếng anh lớp 10 Explore new worlds
Giải bài tập sách bài tập (SBT) lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tin học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Global success
Giải bài tập sách bài tập (SBT) lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 chân trời sáng tạo bản 1
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 chân trời sáng tạo bản 2
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Friends Global
Giải bài tập sách bài tập (SBT) lớp 10 Cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) tin học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Explore new world
Giải bài tập chuyên đề học tập 10 Kết nối tri thức
- Giải bài tập chuyên đề toán lớp 10 kết nối tri thức
- Giải bài tập chuyên đề ngữ văn lớp 10 kết nối tri thức
- Giải bài tập chuyên đề vật lí lớp 10 kết nối tri thức
- Giải bài tập chuyên đề hóa học lớp 10 kết nối tri thức
- Giải bài tập chuyên đề sinh học lớp 10 kết nối tri thức
- Giải bài tập chuyên đề lịch sử lớp 10 kết nối tri thức
- Giải bài tập chuyên đề địa lí lớp 10 kết nối tri thức
- Giải bài tập chuyên đề công nghệ trồng trọt lớp 10 kết nối tri thức
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng tin học ứng dụng kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng khoa học máy tính kết nối tri thức
- Giải bài tập chuyên đề mĩ thuật lớp 10 kết nối tri thức
Giải bài tập chuyên đề học tập 10 Chân trời sáng tạo
- Giải bài tập chuyên đề toán lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề ngữ văn lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề vật lí lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề hóa học lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề sinh học lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề địa lí lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề âm nhạc lớp 10 chân trời sáng tạo
Giải bài tập chuyên đề học tập 10 Cánh diều
- Giải bài tập chuyên đề toán lớp 10 cánh diều
- Giải bài tập chuyên đề ngữ văn lớp 10 cánh diều
- Giải bài tập chuyên đề vật lí lớp 10 cánh diều
- Giải bài tập chuyên đề hóa học lớp 10 cánh diều
- Giải bài tập chuyên đề sinh học lớp 10 cánh diều
- Giải bài tập chuyên đề địa lí lớp 10 cánh diều
- Giải bài tập chuyên đề lịch sử lớp 10 cánh diều
- Giải bài tập chuyên đề công nghệ trồng trọt lớp 10 cánh diều
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 cánh diều
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng tin học ứng dụng cánh diều
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng khoa học máy tính cánh diều
- Giải bài tập chuyên đề âm nhạc lớp 10 cánh diều




