CHƯƠNG 1: CÁC LOẠI HỢP CHẤT VÔ CƠ
- Giải bài tập 1: Tính chất hóa học của oxit. Khái quát về sự phân loại oxit.
- Giải bài tập 2: Một số oxit quan trọng (Tiết 1)
- Giải bài tập 2: Một số oxit quan trọng - Tiết 2
- Giải bài tập 3: Tính chất hóa học của axit
- Giải bài tập 4: Một số axit quan trọng
- Giải bài tập 5: Luyện tập - Tính chất hóa học của oxit và axit
- Giải bài tập 6: Thực hành - Tính chất hóa học của oxit và axit
- Giải bài tập 7: Tính chất hóa học của bazơ
- Giải bài tập 8: Một số bazơ quan trọng - Tiết 1
- Giải bài tập 8: Một số bazơ quan trọng - Tiết 2
- Giải bài tập 9: Tính chất hóa học của muối
- Giải bài tập 10: Một số muối quan trọng
- Giải bài tập 11: Phân bón hóa học
- Giải bài tập 12: Mối quan hệ giữa các loại hợp chất vô cơ
- Giải bài tập 13: Luyện tập chương 1- Các loại hợp chất vô cơ
CHƯƠNG 2: KIM LOẠI
- Giải bài tập 14: Thực hành - Tính chất hóa học của bazơ và muối
- Giải bài tập 17: Dãy hoạt động hóa học của kim loại
- Giải bài tập 18: Nhôm
- Giải bài tập 19: Sắt
- Giải bài tập 20: Hợp kim sắt: Gang, thép
- Giải bài tập 21: Sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn
- Giải bài tập 22: Luyện tập chương 2 - Kim loại
- Giải bài tập 23: Thực hành Tính chất hóa học của nhôm và sắt
- Giải bài tập 24: Ôn tập học kì 1
CHƯƠNG 3: PHI KIM - SƠ LƯỢC VỀ BẢNG TUẦN HOÀN VÀ CÁC NGUYÊN TỐ HÓA HỌC
- Giải bài tập 25: Tính chất hóa học của phi kim
- Giải bài tập 26: Clo
- Giải bài tập 27: Cacbon
- Giải bài tập 28: Các oxit của cacbon
- Giải bài tập 29: Axit cacbonic và muối cacbonat
- Giải bài tập 30: Silic. Công nghiệp silicat
- Giải bài tập 31: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập 32: Luyện tập chương 3: Phi kim Sơ lược về bảng tuần hoàn các nguyên tố đã học
- Giải bài tập 33: Thực hành: Tính chất hóa học của phi kim và hợp chất của chúng
CHƯƠNG 4: HIDROCACBON. NHIÊN LIỆU
- Giải bài tập 34: Khái niệm về hợp chất hữu cơ và hóa học hữu cơ
- Giải bài tập 35: Cấu tạo phân tử hợp chất hữu cơ
- Giải bài tập 36: Metan
- Giải bài tập 37: Etilen
- Giải bài tập 38 hoá học 9: Axetilen
- Giải bài tập 39 hoá học 9: Benzen
- Giải bài tập 40 hoá học 9: Dầu mỏ và khí thiên nhiên
- Giải bài tập 41 hoá học 9: Nhiên liệu
- Giải bài tập 42 hoá học 9: Luyện tập chương 4: Hiđrocacbon - Nhiên liệu
- Giải bài tập 43 hoá học 9: Thực hành: Tính chất hóa học của hiđrocacbon
CHƯƠNG 5: DẪN XUẤT CỦA HIDROCACBON. POLIME
- Giải bài tập 44: Rượu etylic
- Giải bài tập 45: Axit axetic
- Giải bài tập 46: Mối liên hệ giữa etilen, rượu etylic và axit axetic
- Giải bài tập 47: Chất béo
- Giải bài tập 49: Thực hành: Tính chất của rượu và axit
- Giải bài tập 50: Glucozơ
- Giải bài tập 51: Saccarozơ
- Giải bài tập 48: Luyện tập: Rượu etylic, axit axetic và chất béo
- Giải bài tập 52: Tinh bột và xenlulozơ
- Giải bài tập 53: Protein
- Giải bài tập 54: Polime
- Giải bài tập 55: Thực hành: Tính chất của gluxit
- Giải bài tập 56: Ôn tập cuối năm - Phần 1
- Giải bài tập 56: Ôn tập cuối năm - Phần 2
Giải bài tập 23: Thực hành Tính chất hóa học của nhôm và sắt
https://s.shopee.vn/6Ai1QhN7jj
Bài học về tính chất hóa học của nhôm và sắt
Trên thực tế, chúng ta thường áp dụng kiến thức lý thuyết vào thực hành để hiểu rõ hơn về tính chất hóa học của các nguyên tố. Trong bài học này, chúng ta sẽ tìm hiểu về hai nguyên tố quan trọng là nhôm và sắt.
1. Tính chất hóa học của nhôm:
a. Tác dụng với phi kim:
- Phản ứng với oxi tạo thành oxit:
4Al + 3O2 $\overset{t^{0}}{\rightarrow}$ 2Al2O3 - Phản ứng với phi kim khác tạo thành muối:
2Al + 3Cl2 $\overset{t^{0}}{\rightarrow}$ 2AlCl3
b. Tác dụng với dung dịch axit:
Tạo thành muối và giải phóng khí H2:
2Al + 6HCl $\rightarrow$ 2AlCl3 + 3H2↑
c. Tác dụng với dung dịch muối:
- Nhôm có thể tạo ra phản ứng với dung dịch muối của các kim loại khác.
- Nhôm cũng có thể phản ứng với dung dịch kiềm, tạo ra muối kiềm và giải phóng khí H2.
2. Tính chất hóa học của sắt:
a. Tác dụng với phi kim:
- Tác dụng với oxi tạo ra oxit sắt:
3Fe + 2O2 $\overset{t^{0}}{\rightarrow}$ Fe3O4 - Tác dụng với clo tạo thành sắt (III) clorua:
2Fe + 3Cl2 $\overset{t^{0}}{\rightarrow}$ 2FeCl3
b. Tác dụng với dung dịch axit:
Tạo thành muối sắt (II) và giải phóng khí H2:
Fe + 2HCl $\rightarrow$ FeCl2 + H2↑
c. Tác dụng với dung dịch muối:
- Sắt tác dụng với dung dịch muối của các kim loại kém hoạt động hơn, tạo ra muối mới và kim loại khác.
Trên cơ sở lý thuyết và thực hành, chúng ta đã tìm hiểu về tính chất hóa học của nhôm và sắt thông qua các phản ứng hoá học xuất phát từ việc tác dụng với các chất khác nhau. Hi vọng rằng, kiến thức này sẽ giúp bạn hiểu rõ hơn về hai nguyên tố quan trọng này.
Bài tập và hướng dẫn giải
Thí nghiệm 1: Tác dụng của nhôm với oxi
Lấy một ít bột nhôm rắc nhẹ bột nhôm trên ngọn lửa đèn cồn (hình 2.10 trang 55)
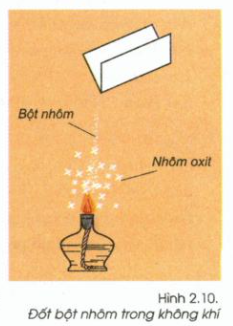
- Quan sát hiện tượng xảy ra.
- Cho biết trạng thái, màu sắc của chất tạo thành, giải thích và viết phương trình hóa học.
- Cho biết vai trò của nhôm trong phản ứng
Thí nghiệm 2: Tác dụng của sắt với lưu huỳnh
Lấy một thìa nhỏ hỗn hợp bột sắt và bột lưu huỳnh theo tỉ lệ 7 : 4 về khối lượng vào ống nghiệm. Đun ống nghiệm trên ngọn lửa đèn cồn (hình 2.20).

- Quan sát hiện tượng. Cho biết màu sắc của sắt, lưu huỳnh, hỗn hợp bột (sắt + lưu huỳnh) và chất tạo thành sau phản ứng
- Giải thích và viết phương trình hóa học.
Thí nghiệm 3: Nhận biết kim loại Al, Fe
Lấy một ít bột kim loại Al, Fe và hai ống nghiệm (1) và (2).
Nhỏ 4 - 5 giọt dung dịch NaOH vào từng ống nghiệm (1) và (2).
- Quan sát hiện tượng xảy ra.
- Cho biết mỗi lọ đựng kim loại nào? Hãy giải thích
Giải bài tập sách giáo khoa (SGK) lớp 9
- Soạn văn lớp 9 tập 1
- Soạn văn lớp 9 tập 2
- Soạn văn lớp 9 tập 1 giản lược
- Soạn văn lớp 9 tập 2 giản lược
- Giải bài tập sách giáo khoa (SGK) toán lớp 9 tập 1
- Giải bài tập sách giáo khoa (SGK) toán lớp 9 tập 2
- Giải bài tập sách giáo khoa (SGK) sinh học lớp 9
- Giải bài tập sách giáo khoa (SGK) hoá học lớp 9
- Giải bài tập sách giáo khoa (SGK) vật lí lớp 9
- Giải bài tập sách giáo khoa (SGK) địa lí lớp 9
- Giải bài tập sách giáo khoa (SGK) lịch sử lớp 9
- Giải bài tập sách giáo khoa (SGK) gdcd lớp 9
- Giải bài tập sách giáo khoa (SGK) tiếng anh lớp 9
- Giải bài tập mĩ thuật lớp 9 Đan Mạch
Giải bài tập sách giáo khoa (SGK) lớp 9 VNEN
- Soạn văn lớp 9 tập 1 VNEN
- Soạn văn lớp 9 tập 2 VNEN
- Soạn văn lớp 9 VNEN siêu ngắn
- Soạn văn lớp 9 VNEN tập 1 giản lược
- Soạn văn lớp 9 VNEN tập 2 giản lược
- Giải bài tập toán lớp 9 tập 1 VNEN
- Giải bài tập toán lớp 9 tâp 2 VNEN
- Giải bài tập khoa học tự nhiên lớp 9
- Giải bài tập khoa học xã hội lớp 9
- Giải bài tập gdcd lớp 9 VNEN
- Giải bài tập công nghệ lớp 9 VNEN
- Giải bài tập tin học lớp 9 VNEN
- Giải bài tập tiếng anh lớp 9 mới - Tập 1
- Giải bài tập tiếng anh lớp 9 mới - Tập 2
Tài liệu lớp 9
- Văn mẫu lớp 9
- Đề thi lên 10 Toán
- Đề thi môn Hóa lớp 9
- Đề thi môn Địa lớp 9
- Đề thi môn vật lí lớp 9
- Tập bản đồ địa lí lớp 9
- Ôn toán lớp 9 lên 10
- Ôn Ngữ văn lớp 9 lên 10
- Ôn tiếng anh lớp 9 lên 10
- Đề thi lên 10 chuyên Toán
- Chuyên đề ôn tập Hóa lớp 9
- Chuyên đề ôn tập Sử lớp 9
- Chuyên đề toán lớp 9
- Chuyên đề Địa Lý lớp 9
- Phát triển năng lực toán lớp 9 tập 1
- Bài tập phát triển năng lực toán lớp 9




