CHƯƠNG 1. CÂN BẰNG HÓA HỌC
CHƯƠNG 2. NITROGEN - SULFUR
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 4 Nitrogen
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 5 Ammonia - Muối Ammonium
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 6 Một số hợp chất của Nitrogen với Oxygen
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 7 Sulfur và sulfur dioxide
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 8 Sulfuric acid và muối sulfate
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 9 Ôn tập chương 2
CHƯƠNG 3. ĐẠI CƯƠNG VỀ HÓA HỌC HỮU CƠ
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 10 Hợp chất hữu cơ và hóa học hữu cơ
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 11 Phương pháp tách biệt và phương tinh chế hợp chất hữu cơ
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 12 Công thức phân tử hợp chất hữu cơ
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 13 Cấu tạo hóa học hợp chất hữu cơ
- Giải bài tập hóa học lớp 11 kết nối tri thức bài 14 Ôn tập chương 3
CHƯƠNG 4. HYDROCARBON
CHƯƠNG 5. DẪN XUẤT HALOGEN - ALCOHOL - PHENOL
Giải bài tập hóa học lớp 11 kết nối tri thức bài 5 Ammonia - Muối Ammonium
https://s.shopee.vn/2LVIrhIyVS
Giải bài 5: Ammonia - Muối Ammonium
Trong sách hóa học lớp 11 kết nối tri thức, phần bài tập về Ammonia - Muối Ammonium được giải đáp chi tiết và cụ thể. Những câu hỏi trong chương trình học được giải thích rõ ràng, giúp các em học sinh hiểu rõ hơn về chủ đề này.
Đáp án chuẩn và hướng dẫn giải cụ thể giúp học sinh nắm vững kiến thức bài học. Mong rằng, sau khi đọc sách này, các em sẽ tự tin hơn khi giải các bài tập liên quan đến Ammonia - Muối Ammonium.
Bài tập và hướng dẫn giải
MỞ ĐẦU
Từ ammonia, thông qua phản ứng nào có thể sản xuất phân đạm chứa ion ammonium? Ammonia đóng vai trò gì trong phản ứng đó?
I. AMMONIA
1. Cấu tạo phân tử
Hoạt động nghiên cứu:
1. Viết cấu hình electron của các nguyên tử H (Z = 1) và N (Z = 7).
2. Trình bày các bước lập công thức Lewis của phân tử ammonia.
Câu hỏi 1: Từ đặc điểm cấu tạo của phân tử ammonia, hãy giải thích tại sao các phân tử ammonia có khả năng tạo liên kết hydrogen mạnh với nhau.
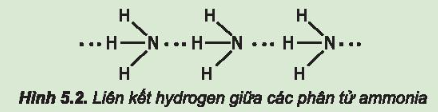
2. Tính chất vật lí
Câu hỏi 2: Hãy giải thích tại sao ammonia tan tốt trong nước.
3. Tính chất hóa học
Hoạt động nghiên cứu: Trong công nghiệp, phản ứng giữa ammonia với acid được dùng để sản xuất phân bón:
NH3 + HCl → NH4CI
NH3 + HNO3 → NH4NO3
2NH3 + H2SO4 → (NH4)2SO4
Xác định chất cho, chất nhận proton trong mỗi phản ứng trên. Dùng mũi tên để biểu diễn sự cho, nhận đó.
Câu hỏi 3: Trong hai phản ứng oxi hóa ammonia bằng oxygen ở trên, hãy:
a) Xác định các nguyên tử có sự thay đổi số oxi hóa.
b) Viết quá trình oxi hóa, quá trình khử.
4. Ứng dụng
Hoạt động nghiên cứu: Sưu tầm một số hình ảnh đề báo cáo, thuyết trình về ứng dụng của ammonia trong thực tiễn. Sử dụng các tính chất vật Ií và hoá học để giải thích cơ sở khoa học của các ứng dụng này.
5. Sản xuất
Hoạt động nghiên cứu: Vận dụng kiến thức về cân bằng hóa học, tốc độ phản ứng, biến thiên enthalpy để giải thích các điều kiện của phản ứng sản xuất ammonia, cụ thể:
1. Nếu tăng hoặc giảm nhiệt độ sẽ ảnh hưởng đến sự chuyển dịch cân bằng và tốc độ phản ứng như thế nào?
2. Nếu giảm áp suất, cân bằng chuyển dịch theo chiều nào? Tại sao không thực hiện ở áp suất cao hơn?
3. Vai trò của chất xúc tác trong phản ứng là gì?
II. MUỐI AMMONIUM
Hoạt động thực hành:
Thí nghiệm: Nhận biết ion ammonium trong phân đạm
Chuẩn bị: phân bón potassium nitrate và phân bón ammonium chloride dạng rắn, dung dịch NaOH 20%, giấy pH; bình xịt tia nước cất, 2 ống nghiệm, kẹp gỗ, đèn cồn. Tiến hành:
- Cho khoảng 1 g phân bón potassium nitrate vào ống nghiệm (1) và khoảng 1 g phân bón ammonium chloride vào ống nghiệm (2).
- Thêm vào mỗi ống nghiệm khoảng 3 mL nước cất, lắc đều cho tan hết.
- Nhỏ 1 mL dung dịch NaOH 20% vào mỗi ống nghiệm, đun nóng nhẹ trên đèn cồn.
- Đưa hai mẫu giấy pH đã tẩm ướt vào miệng mỗi ống nghiệm.
Quan sát hiện tượng và trả lời câu hỏi:
Dựa vào dấu hiệu nào để nhận biết ion ammonium? Giải thích bằng phương trình hoá học.
Câu hỏi 4: a) So sánh phân tử ammonia và ion ammonium về dạng hình học, số liên kết cộng hóa trị, số oxi hóa của nguyên tử nitrogen.
b) Viết phương trình hóa học minh họa tính acid/base của ammonia và ammonium.
Giải bài tập sách giáo khoa (SGK) lớp 11 kết nối tri thức
- Soạn ngữ văn lớp 11 kết nối tri thức
- Văn mẫu lớp 11 kết nối tri thức
- Soạn ngữ văn lớp 11 tập 1 kết nối tri thức
- Soạn ngữ văn lớp 11 tập 2 kết nối tri thức
- Giải bài tập toán lớp 11 tập 1 kết nối tri thức
- Giải bài tập toán lớp 11 tập 2 kết nối tri thức
- Giải bài tập vật lí lớp 11 kết nối tri thức
- Giải bài tập hóa học lớp 11 kết nối tri thức
- Giải bài tập sinh học lớp 11 kết nối tri thức
- Giải bài tập lịch sử lớp 11 kết nối tri thức
- Giải bài tập địa lí lớp 11 kết nối tri thức
- Giải bài tập kinh tế pháp luật lớp 11 kết nối tri thức
- Giải bài tập âm nhạc lớp 11 kết nối tri thức
- Giải bài tập mĩ thuật lớp 11 kết nối tri thức
- Giải bài tập quốc phòng an ninh lớp 11 kết nối tri thức
- Giải bài tập công nghệ chăn nuôi lớp 11 kết nối tri thức
- Giải bài tập công nghệ cơ khí lớp 11 kết nối tri thức
- Giải bài tập tin học lớp 11 định hướng Tin học ứng dụng kết nối tri thức
- Giải bài tập tin học lớp 11 định hướng Khoa học máy tính kết nối tri thức
- Giải bài tập hoạt động trải nghiệm hướng nghiệp lớp 11 kết nối tri thức
Giải bài tập sách giáo khoa (SGK) lớp 11 chân trời sáng tạo
- Soạn ngữ văn lớp 11 chân trời sáng tạo
- Văn mẫu lớp 11 chân trời sáng tạo
- Soạn ngữ văn lớp 11 tập 1 chân trời sáng tạo
- Soạn ngữ văn lớp 11 tập 2 chân trời sáng tạo
- Giải bài tập toán lớp 11 tập 1 chân trời sáng tạo
- Giải bài tập toán lớp 11 tập 2 chân trời sáng tạo
- Giải bài tập vật lí lớp 11 chân trời sáng tạo
- Giải bài tập hóa học lớp 11 chân trời sáng tạo
- Giải bài tập sinh học lớp 11 chân trời sáng tạo
- Giải bài tập lịch sử lớp 11 chân trời sáng tạo
- Giải bài tập địa lí lớp 11 chân trời sáng tạo
- Giải bài tập kinh tế pháp luật lớp 11 chân trời sáng tạo
- Giải bài tập âm nhạc lớp 11 chân trời sáng tạo
- Giải bài tập mĩ thuật lớp 11 chân trời sáng tạo
- Giải bài tập quốc phòng an ninh lớp 11 chân trời sáng tạo
- Giải bài tập hoạt động trải nghiệm hướng nghiệp lớp 11 chân trời sáng tạo bản 1
- Giải bài tập hoạt động trải nghiệm hướng nghiệp lớp 11 chân trời sáng tạo bản 2
Giải bài tập sách giáo khoa (SGK) lớp 11 cánh diều
- Soạn ngữ văn lớp 11 cánh diều
- Văn mẫu lớp 11 cánh diều
- Soạn ngữ văn lớp 11 tập 1 cánh diều
- Soạn ngữ văn lớp 11 tập 2 cánh diều
- Giải bài tập toán lớp 11 tập 1 cánh diều
- Giải bài tập toán lớp 11 tập 2 cánh diều
- Giải bài tập vật lí lớp 11 cánh diều
- Giải bài tập hóa học lớp 11 cánh diều
- Giải bài tập sinh học lớp 11 cánh diều
- Giải bài tập lịch sử lớp 11 cánh diều
- Giải bài tập địa lí lớp 11 cánh diều
- Giải bài tập kinh tế pháp luật lớp 11 cánh diều
- Giải bài tập âm nhạc lớp 11 cánh diều
- Giải bài tập mĩ thuật lớp 11 cánh diều
- Giải bài tập quốc phòng an ninh lớp 11 cánh diều
- Giải bài tập công nghệ chăn nuôi lớp 11 cánh diều
- Giải bài tập công nghệ cơ khí lớp 11 cánh diều
- Giải bài tập tin học lớp 11 định hướng Tin học ứng dụng cánh diều
- Giải bài tập tin học lớp 11 định hướng Khoa học máy tính cánh diều
- Giải bài tập hoạt động trải nghiệm hướng nghiệp lớp 11 cánh diều
Giải bài tập sách bài tập (SBT) lớp 11 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 11 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 11 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 11 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 11 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) sinh học lớp 11 kết nối tri thức
- Giải bài tập sách bài tập (SBT) vật lí lớp 11 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hóa học lớp 11 kết nối tri thức
- Giải bài tập sách bài tập (SBT) địa lí lớp 11 kết nối tri thức
- Giải bài tập sách bài tập (SBT) lịch sử lớp 11 kết nối tri thức
- Giải bài tập sách bài tập (SBT) kinh tế pháp luật lớp 11 kết nối tri thức
- Giải bài tập sách bài tập (SBT) quốc phòng an ninh lớp 11 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm hướng nghiệp lớp 11 kết nối tri thức
Giải bài tập sách bài tập (SBT) lớp 11 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 11 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 11 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 11 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 11 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) sinh học lớp 11 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) vật lí lớp 11 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hóa học lớp 11 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) lịch sử lớp 11 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) địa lí lớp 11 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) kinh tế pháp luật lớp 11 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) quốc phòng an ninh lớp 11 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm hướng nghiệp lớp 11 chân trời sáng tạo bản 1
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm hướng nghiệp lớp 11 chân trời sáng tạo bản 2
Giải bài tập sách bài tập (SBT) lớp 11 cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 11 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 11 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 11 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 11 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) vật lí lớp 11 cánh diều
- Giải bài tập sách bài tập (SBT) sinh học lớp 11 cánh diều
- Giải bài tập sách bài tập (SBT) hóa học lớp 11 cánh diều
- Giải bài tập sách bài tập (SBT) địa lí lớp 11 cánh diều
- Giải bài tập sách bài tập (SBT) lịch sử lớp 11 cánh diều
- Giải bài tập sách bài tập (SBT) kinh tế pháp luật lớp 11 cánh diều
- Giải bài tập sách bài tập (SBT) quốc phòng an ninh lớp 11 cánh diều
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm hướng nghiệp lớp 11 cánh diều
Giải bài tập chuyên đề học tập lớp 11 kết nối tri thức
- Giải bài tập chuyên đề toán lớp 11 kết nối tri thức
- Giải bài tập chuyên đề ngữ văn lớp 11 kết nối tri thức
- Giải bài tập chuyên đề vật lí lớp 11 kết nối tri thức
- Giải bài tập chuyên đề hóa học lớp 11 kết nối tri thức
- Giải bài tập chuyên đề sinh học lớp 11 kết nối tri thức
- Giải bài tập chuyên đề kinh tế pháp luật lớp 11 kết nối tri thức
- Giải bài tập chuyên đề lịch sử lớp 11 kết nối tri thức
- Giải bài tập chuyên đề địa lí lớp 11 kết nối tri thức
- Giải bài tập chuyên đề mĩ thuật lớp 11 kết nối tri thức
- Giải bài tập chuyên đề âm nhạc lớp 11 kết nối tri thức
- Giải bài tập chuyên đề công nghệ chăn nuôi lớp 11 kết nối tri thức
- Giải bài tập chuyên đề công nghệ cơ khí lớp 11 kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 11 định hướng Khoa học máy tính kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 11 định hướng Tin học ứng dụng kết nối tri thức
- Giải bài tập chuyên đề quốc phòng an ninh lớp 11 kết nối tri thức
- Giải bài tập chuyên đề hoạt động trải nghiệm hướng nghiệp lớp 11 kết nối tri thức
Giải bài tập chuyên đề học tập lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề toán lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề ngữ văn lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề vật lí lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề hóa học lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề sinh học lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề lịch sử lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề địa lí lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề âm nhạc lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề mĩ thuật lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề kinh tế pháp luật lớp 11 chân trời sáng tạo
- Giải bài tập chuyên đề hoạt động trải nghiệm hướng nghiệp lớp 11 chân trời sáng tạo bản 1
- Giải bài tập chuyên đề hoạt động trải nghiệm hướng nghiệp lớp 11 chân trời sáng tạo bản 2
- Giải bài tập chuyên đề quốc phòng an ninh lớp 11 chân trời sáng tạo
Giải bài tập chuyên đề học tập lớp 11 cánh diều
- Giải bài tập chuyên đề toán lớp 11 cánh diều
- Giải bài tập chuyên đề ngữ văn lớp 11 cánh diều
- Giải bài tập chuyên đề vật lí lớp 11 cánh diều
- Giải bài tập chuyên đề hóa học lớp 11 cánh diều
- Giải bài tập chuyên đề sinh học lớp 11 cánh diều
- Giải bài tập chuyên đề lịch sử lớp 11 cánh diều
- Giải bài tập chuyên đề địa lí lớp 11 cánh diều
- Giải bài tập chuyên đề kinh tế pháp luật lớp 11 cánh diều
- Giải bài tập chuyên đề mĩ thuật lớp 11 cánh diều
- Giải bài tập chuyên đề âm nhạc lớp 11 cánh diều
- Giải bài tập chuyên đề công nghệ chăn nuôi lớp 11 cánh diều
- Giải bài tập chuyên đề công nghệ cơ khí lớp 11 cánh diều
- Giải bài tập chuyên đề tin học lớp 11 định hướng Tin học ứng dụng cánh diều
- Giải bài tập chuyên đề tin học lớp 11 định hướng Khoa học máy tính cánh diều
- Giải bài tập chuyên đề quốc phòng an ninh lớp 11 cánh diều
- Giải bài tập chuyên đề hoạt động trải nghiệm hướng nghiệp lớp 11 cánh diều




