16.12.Bạn A và B thực hiện phản ứng giữa kẽm với dung dịch hydrocloric acid và thu được thể...
16.12. Bạn A và B thực hiện phản ứng giữa kẽm với dung dịch hydrocloric acid và thu được thể tích khí thoát ra theo thời gian. Hai bạn lặp lại thí nghiệm ba lần và kết quả của ba lần thí nghiệm được hai bạn ghi vào bảng sau:
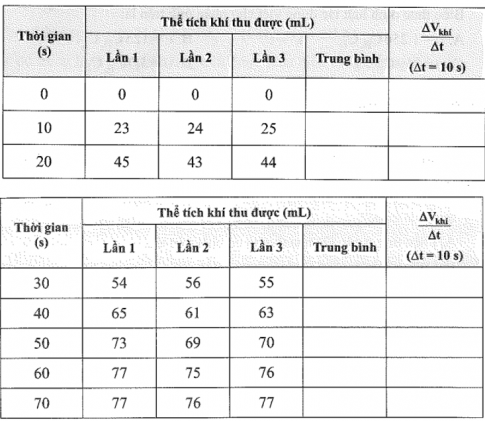
a) Cho biết khí thoát ra là khí gì. Hãy viết và cân bằng phương trình hoá học của phản ứng xảy ra.
b) Hoàn thành hai cột còn trống trong bảng trên. Hãy biểu diễn kết quả của hai bạn lên đồ thị thể tích khí thu được theo thời gian. Vì sao hai bạn lại lặp lại thí nghiệm ba lần?
c) Dựa vào đồ thị, cho biết khi nào phản ứng kết thúc. Vì sao?
d) Phản ứng diễn ra nhanh nhất trong khoảng thời gian nào? Sau đó, phản ứng diễn ra nhanh dần hay chậm dần?
e) Nếu thí nghiệm được lặp lại với nồng độ HCl lớn hơn thì tốc độ phản ứng sẽ nhanh hơn hay chậm hơn?
g) Nếu hai bạn không đo được thể tích khí thoát ra, em hãy đề xuất một cách khác để xác định tốc độ phản ứng.
- 16.1.Những phát biểu nào sau đây là đúng?A. Tốc độ của phản ứng hoá học là đại lượng mô tả...
- 16.2.Những phát biểu nào sau đâykhông đúng?A. Tốc độ của phản ứng hoá học chỉ có thể...
- 16.3.Khi cho một lượng xác định chất phản ứng vào bình để cho phản ứng hoá học xảy ra, tốc độ...
- 16.4.Tốc độ phản ứng còn được tính theo sự thay đổi lượng chất (số mol, khối lượng) theo thời...
- 16.5.Cho hai phản ứng có phương trình hóa học như sau:2O3 (g)→ 3O2 (g) (1)2HOF...
- 16.6.Phản ứng 3H2+ N2→ 2NH3có tốc độ mất đi của H2so với tốc độ hình...
- 16.7.Cho phản ứng:6CH2O + 4NH3→ (CH2)6N4+ 6H2OTốc độ trung bình của phản ứng trên...
- 16.8.Những phát biểu nào sau đây không đúng?A. Phản ứng đơn giản là phản ứng xảy ra theo một...
- 16.9.Cho phản ứng đơn giản:H2+ I2→ 2HINgười ta thực hiện ba thí nghiệm với nồng...
- 16.10.Cho phản ứng:2A + B → 2M + 3Na) Hãy viết biểu thức tính tốc độ trung bình của phản ứng...
- 16.11.Phản ứng A → 2B được thực hiện trong một bình phản ứng. Số liệu thực nghiệm của phản...
- 16.13.Một phản ứng có hệ số nhiệt độ Van’t Hoff bằng 3,5. Ở 15 °C, tốc độ của phản ứng này...
- 16.14.Một bạn học sinh thực hiện hai thí nghiệm:Thí nghiệm 1:Cho 100 mL dung dịch acid...
- 16.15.Khi tăng áp suất của chất phản ứng, tốc độ của những phản ứng nào sau đây sẽ bị thay...
- 16.16.Khi nghiên cứu ảnh hưởng của nhiệt độ tới tốc độ của phản ứng giữa Mg(s) với HCl(aq),...
- 16.17.Từ một miếng đá vôi và một lọ dung dịch HCl 1 M, thí nghiệm được tiến hành trong điều...
- 16.18.Chất xúc tác là chấtA. làm tăng tốc độ phản ứng và không bị mất đi sau phản ứng.B. làm...
- 16.19.Enzyme catalase phân huỷ hydrogen peroxide thành oxygen và nước nhanh gấp khoảng 1...
- 16.20.Hai bạn Tôm và Vừng thực hiện một thí nghiệm về sự phân huỷ của hydrogen peroxide với...




