SBT CHƯƠNG 1: CẤU TẠO CỦA NGUYÊN TỬ
SBT CHƯƠNG 2: BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC VÀ ĐỊNH LUẬT TUẦN HOÀN
- Giải bài tập sách bài tập (SBT) bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một chu kì và trong một nhóm
- Giải bài tập sách bài tập (SBT) bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
- Giải bài tập sách bài tập (SBT) bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
- Giải bài tập sách bài tập (SBT) bài 9: Ôn tập chương 2
SBT CHƯƠNG 3: LIÊN KẾT HÓA HỌC
- Giải bài tập sách bài tập (SBT) bài 10 Quy tắc Octet
- Giải bài tập sách bài tập (SBT) bài 11 Liên kết ion
- Giải bài tập sách bài tập (SBT) bài 12 Liên kết cộng hóa trị
- Giải bài tập sách bài tập (SBT) Hoá 10 kết nối tri thức bài 13: Liên kết Hydrogen và tương tác Van Der Waals
- Giải bài tập sách bài tập (SBT) Hoá 10 kết nối tri thức bài 14: Ôn tập chương 3
SBT CHƯƠNG 4: PHẢN ỨNG HÓA HỌC
SBT CHƯƠNG 5: NĂNG LƯỢNG HÓA HỌC
SBT CHƯƠNG 6: TỐC ĐỘ PHẢN ỨNG
Giải bài tập sách bài tập (SBT) Hoá 10 kết nối tri thức bài 21 Nhóm halogen
https://s.shopee.vn/2LVIrhIyVS
Hướng dẫn giải bài 21 Nhóm halogen trang 65 sách bài tập (SBT) Hoá học 10
Bài tập 21 Nhóm halogen trang 65 sách bài tập (SBT) Hoá học 10 là một trong những bài tập được biên soạn theo chương trình đổi mới của Bộ giáo dục. Đây là một bài tập có tính học thuật cao, nhưng cũng mang tính ứng dụng cao trong cuộc sống hàng ngày.
Qua cách hướng dẫn cụ thể và giải chi tiết, học sinh sẽ dễ dàng nắm bắt được kiến thức về nhóm halogen và áp dụng vào các bài tập tương tự. Mong rằng, qua việc giải bài tập này, học sinh sẽ hiểu sâu hơn về chủ đề này và áp dụng được vào thực tế hơn.
Đây thực sự là một cơ hội tuyệt vời để nắm vững kiến thức và rèn luyện kỹ năng giải bài tập của mình. Hãy cố gắng và không ngần ngại hỏi thầy cô hoặc bạn bè nếu gặp khó khăn nhé!
Bài tập và hướng dẫn giải
NHẬN BIẾT
21.1. Số electron ở lớp ngoài cùng của mỗi nguyên tử nguyên tố halogen là
A. 5. B. 7. C. 2. D. 8.
21.2. Tính chất hoá học đặc trưng của các đơn chất halogen là
A. tính khử. B. tính base.
C. tính acid. D. tính oxi hoá.
21.3. Trong tự nhiên, nguyên tố fluorine tồn tại phổ biến nhất ở dạng hợp chất là
A. Na3AlF6 B. NaF. C. HF. D. CaF2.
21.4. Ở điều kiện thưởng, halogen tồn tại ở thể rắn, có màu đen tím là
A. F2. B. Br2. C. I2. D. Cl2.
21.5. Muối nào có nhiều nhất trong nước biển với nồng độ khoảng 3%?
A. NaCl. B. KCl. C. MgCl2. D. NaF.
21.6. Số oxi hoá cao nhất mà nguyên tử chlorine thể hiện được trong các hợp chất là
A. -1. B. +7. C. +5. D. +1.
21.7. Các nguyên tố halogen thuộc nhóm nào trong bảng tuần hoàn?
A. VIIIA. B. VIA C. VIIA. D. IIA.
21.8. Trong nhóm halogen, đơn chất có tính oxi hoá mạnh nhất là
A. F2. B. Cl2. C. Br2. D. I2.
21.9. Khi đun nóng, chất thăng hoa chuyển từ thể rắn sang thể hơi màu tím là
A. F2. B. Cl2. C. Br2. D. I2
21.10. Halogen nào sau đây được dùng để khử trùng nước sinh hoạt ?
A. F2. B. Cl2. C. Br2. D. I2.
21.11. Trong cơ thể người, nguyên tố iodine tập trung ở tuyến nào sau đây?
A. Tuyến thượng thận. B. Tuyến tuy.
C. Tuyến yên. D. Tuyến giáp trạng.
21.12. Trong dãy halogen, nguyên tử có độ âm điện nhỏ nhất là
A. fluorine. B. chlorine. C. bromine. D. iodine.
THÔNG HIỂU
21.13. Trong nhóm halogen, từ fluorine đến iodine, bán kính nguyên tử biến đổi như thế nào?
A. Giảm dần. B. Không đổi.
C. Tăng dần. D. Tuần hoàn.
21.14. Trong nhóm halogen, nguyên tử nguyên tố thể hiện khuynh hướng nhận 1 electron yếu nhất là
A. fluorine. B. chlorine.
C. bromine. D. iodine.
21.15. Trong nhóm halogen, từ fluorine đến iodine, nhiệt độ nóng chảy biến đổi như thế nào?
A. Giảm dần. B. Tăng dần.
C. Không đổi. D. Tuần hoàn.
21.16. Halogen phản ứng mãnh liệt với hydrogen ngay cả trong bóng tối là
A. F2. B. Cl2. C. Br2. D. I2.
21.17. Khi tác dụng với kim loại, các nguyên tử halogen thể hiện xu hướng nào sau đây?
A. Nhường 1 electron. B. Nhận 1 electron.
C. Nhường 7 electron. D. Góp chung 1 electron.
21.18. Hít thở không khí có chứa khí nào sau đây vượt ngưỡng 30 μg/$m^{3}$ không khí (QCVN 06:2009/BTNMT) sẽ tiềm ẩn nguy cơ gây co thắt phế quản, khó thở?
A. O2 B. Cl2 C. N2 D. O3
21.19. Quá trình sản xuất khí chlorine trong công nghiệp hiện nay dựa trên phản ứng nào sau đây?
A. MnO2 + 4HCl $\underrightarrow{t^{o}}$ MnCl2 + Cl2 + 2H2O.
B. Cl2 + 2NaBr → 2NaCl + Br2.
C. 2NaCl + 2H2O $\underrightarrow{đpdd cmn}$ 2NaOH + Cl2 + H2.
D. 2NaOH + Cl2 → NaCl + NaClO + H2O.
21.20. Chỉ thị nào sau đây thường dùng để nhận biết dung dịch I2?
A. Phenolphtalein. B. Hồ tinh bột.
C. Quỳ tím. D. Nước vôi trong.
VẬN DỤNG
21.21. Thực nghiệm cho thấy các phản ứng:
H2 (g) + X2 (g)→ 2HX (g)
trong dãy halogen xảy ra với mức độ giảm dần từ F2 đến I2. Biến thiên enthalpy của các phản ứng thay đổi như thế nào trong dãy trên?
21.22. Đốt cháy hoàn toàn 0,48 g kim loại M (hoá trị II) bằng khí chlorine, thu được 1,332 g muối chloride. Xác định kim loại M.
21.23. Nung nóng một binh bằng thép có chứa 0,04 mol H2 và 0,04 mol Cl2 để thực hiện phản ứng, thu được 0,072 mol khí HCl.
a) Tính hiệu suất của phản ứng tạo thành HCl.
b) Ở cùng nhiệt độ thường, áp suất suất khí trong bình trước và sau phản ứng lần lượt là P1 và P2. Hãy so sánh P1 và P2.
21.24. Có hai ống nghiệm, mỗi ống chứa 2 mL dung dịch muối X của kali. Cho vài giọt dung dịch AgNO3 vào ống thứ nhất, thu được kết tủa màu vàng. Nhỏ vài giọt nước Br2 vào ống thứ hai, lắc đều rồi thêm hồ tinh bột, thấy có màu xanh tím. Xác định công thức hoá học của X và viết phương trình hoá học của các phản ứng.
21.25. Trong phòng thí nghiệm, khí chlorine được điều chế, làm khô và thu vào bình theo sơ đồ dưới đây.
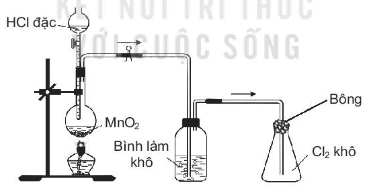
Hãy đề xuất một dung dịch để sử dụng cho từng mục đích sau
a) Cho vào bình làm khô để làm khô khí Cl2.
b) Tẩm vào bông đậy bình thu khí để hạn chế khí Cl2 bay ra.
Giải thích và viết phương trình hoá học minh hoạ nếu có.
Giải bài tập sách giáo khoa (SGK) 10 Kết nối tri thức
- Soạn văn lớp 10 tập 1 kết nối tri thức
- Soạn văn lớp 10 tập 2 kết nối tri thức
- Văn mẫu lớp 10 kết nối tri thức
- Giải bài tập toán lớp 10 tập 1 kết nối tri thức
- Giải bài tập toán lớp 10 tập 2 kết nối tri thức
- Giải bài tập vật lí lớp 10 kết nối tri thức
- Giải bài tập hóa học lớp 10 kết nối tri thức
- Giải bài tập sinh học lớp 10 kết nối tri thức
- Giải bài tập Địa lí lớp 10 kết nối tri thức
- Giải bài tập lịch sử lớp 10 kết nối tri thức
- Giải bài tập tin học lớp 10 kết nối tri thức
- Giải bài tập Âm nhạc lớp 10 kết nối tri thức
- Giải bài tập mĩ thuật lớp 10 kết nối tri thức
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 kết nối tri thức
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 kết nối tri thức
- Giải bài tập hoạt động trải nghiệm lớp 10 kết nối tri thức
- Giải bài tập thiết kế công nghệ lớp 10 kết nối tri thức
- Giải bài tập công nghệ trồng trọt lớp 10 kết nối tri thức
- Giải bài tập giáo dục thể chất lớp 10 kết nối tri thức
- Giải bài tập tiếng anh lớp 10 Global Success
Giải bài tập sách giáo khoa (SGK) 10 Chân trời sáng tạo
- Soạn văn lớp 10 tập 1 chân trời sáng tạo
- Soạn văn lớp 10 tập 2 chân trời sáng tạo
- Văn mẫu lớp 10 chân trời sáng tạo
- Giải bài tập toán lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập toán lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập vật lí lớp 10 chân trời sáng tạo
- Giải bài tập hóa học lớp 10 chân trời sáng tạo
- Giải bài tập sinh học lớp 10 chân trời sáng tạo
- Giải bài tập Địa lí lớp 10 chân trời sáng tạo
- Giải bài tập lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập tin học lớp 10 chân trời sáng tạo
- Giải bài tập Âm nhạc lớp 10 chân trời sáng tạo
- Giải bài tập mĩ thuật lớp 10 chân trời sáng tạo
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập Hoạt động trải nghiệm, hướng nghiệp lớp 10 chân trời sáng tạo bản 1
- Giải bài tập Hoạt động trải nghiệm, hướng nghiệp lớp 10 chân trời sáng tạo bản 2
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 chân trời sáng tạo
- Giải bài tập thiết kế công nghệ lớp 10 chân trời sáng tạo
- Giải bài tập công nghệ trồng trọt lớp 10 chân trời sáng tạo
- Giải bài tập giáo dục thể chất lớp 10 chân trời sáng tạo
- Giải bài tập tiếng anh lớp 10 Friends Global
Giải bài tập sách giáo khoa (SGK) 10 Cánh diều
- Soạn văn lớp 10 tập 1 cánh diều
- Soạn văn lớp 10 tập 2 cánh diều
- Văn mẫu lớp 10 cánh diều
- Giải bài tập toán lớp 10 tập 1 cánh diều
- Giải bài tập toán lớp 10 tập 2 cánh diều
- Giải bài tập vật lí lớp 10 cánh diều
- Giải bài tập hóa học lớp 10 cánh diều
- Giải bài tập sinh học lớp 10 cánh diều
- Giải bài tập Địa lí lớp 10 cánh diều
- Giải bài tập lịch sử lớp 10 cánh diều
- Giải bài tập tin học lớp 10 cánh diều
- Giải bài tập Âm nhạc lớp 10 cánh diều
- Giải bài tập mĩ thuật lớp 10 cánh diều
- Giải bài tập giáo dục kinh tế pháp luật lớp 10 cánh diều
- Giải bài tập giáo dục quốc phòng an ninh lớp 10 cánh diều
- Giải bài tập hoạt động trải nghiệm lớp 10 cánh diều
- Giải bài tập thiết kế công nghệ lớp 10 cánh diều
- Giải bài tập công nghệ trồng trọt lớp 10 cánh diều
- Giải bài tập giáo dục thể chất lớp 10 cánh diều
- Giải bài tập tiếng anh lớp 10 Explore new worlds
Giải bài tập sách bài tập (SBT) lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tin học lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Global success
Giải bài tập sách bài tập (SBT) lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 chân trời sáng tạo bản 1
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 chân trời sáng tạo bản 2
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Friends Global
Giải bài tập sách bài tập (SBT) lớp 10 Cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 10 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 10 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) hóa học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) sinh học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) vật lí lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) lịch sử lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) địa lí lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) tin học lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) giáo dục kinh tế pháp luật lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) giáo dục quốc phòng và an ninh lớp 10 cánh diều
- Giải bài tập sách bài tập (SBT) tiếng anh lớp 10 Explore new world
Giải bài tập chuyên đề học tập 10 Kết nối tri thức
- Giải bài tập chuyên đề toán lớp 10 kết nối tri thức
- Giải bài tập chuyên đề ngữ văn lớp 10 kết nối tri thức
- Giải bài tập chuyên đề vật lí lớp 10 kết nối tri thức
- Giải bài tập chuyên đề hóa học lớp 10 kết nối tri thức
- Giải bài tập chuyên đề sinh học lớp 10 kết nối tri thức
- Giải bài tập chuyên đề lịch sử lớp 10 kết nối tri thức
- Giải bài tập chuyên đề địa lí lớp 10 kết nối tri thức
- Giải bài tập chuyên đề công nghệ trồng trọt lớp 10 kết nối tri thức
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng tin học ứng dụng kết nối tri thức
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng khoa học máy tính kết nối tri thức
- Giải bài tập chuyên đề mĩ thuật lớp 10 kết nối tri thức
Giải bài tập chuyên đề học tập 10 Chân trời sáng tạo
- Giải bài tập chuyên đề toán lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề ngữ văn lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề vật lí lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề hóa học lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề sinh học lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề địa lí lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề lịch sử lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 chân trời sáng tạo
- Giải bài tập chuyên đề âm nhạc lớp 10 chân trời sáng tạo
Giải bài tập chuyên đề học tập 10 Cánh diều
- Giải bài tập chuyên đề toán lớp 10 cánh diều
- Giải bài tập chuyên đề ngữ văn lớp 10 cánh diều
- Giải bài tập chuyên đề vật lí lớp 10 cánh diều
- Giải bài tập chuyên đề hóa học lớp 10 cánh diều
- Giải bài tập chuyên đề sinh học lớp 10 cánh diều
- Giải bài tập chuyên đề địa lí lớp 10 cánh diều
- Giải bài tập chuyên đề lịch sử lớp 10 cánh diều
- Giải bài tập chuyên đề công nghệ trồng trọt lớp 10 cánh diều
- Giải bài tập chuyên đề giáo dục kinh tế và pháp luật lớp 10 cánh diều
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng tin học ứng dụng cánh diều
- Giải bài tập chuyên đề tin học lớp 10 theo định hướng khoa học máy tính cánh diều
- Giải bài tập chuyên đề âm nhạc lớp 10 cánh diều




