CHỦ ĐỀ 1: PHẢN ỨNG HÓA HỌC
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 1 Biến đổi vật lí và biến đổi hóa học
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 2 Phản ứng hóa học và năng lượng của phản ứng hóa học
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 3 Định luật bảo toàn khối lượng Phương trình hoá học
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 4 Mol và tỉ khối của chất khí
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 5 Tính theo phương trình hóa học
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 6 Nồng độ dung dịch
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 7 Tốc độ phản ứng và chất xúc tác
CHỦ ĐỀ 2: ACID - BASE - pH - OXIDE - MUỐI
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 8 Acid
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 9 Base
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 10 Thang pH
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 11 Oxide
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 12 Muối
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 13 Phân bón hoá học
CHỦ ĐỀ 3: KHỐI LƯỢNG RIÊNG VÀ ÁP SUẤT
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 14 Khối lượng riêng
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 15 Tác dụng của chất lỏng đặt lên vật đặt trong nó
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 16 Áp suất
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 17 Áp suất chất lỏng và chất khí
CHỦ ĐỀ 4: TÁC DỤNG LÀM QUAY CỦA LỰC
CHỦ ĐỀ 5: ĐIỆN
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 20 Sự nhiễm điện
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 21 Mạch điện
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 22 Tác dụng của dòng điện
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 23 Cường độ dòng điện và hiệu điện thế
CHỦ ĐỀ 6: NHIỆT
CHỦ ĐỀ 7: CƠ THỂ NGƯỜI
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 27 Khái quát về cơ thể con người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 28 Hệ vận động ở người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 29 Dinh dưỡng và tiêu hoá ở người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 30 Máu và hệ tuần hoàn ở người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 31 Thực hành về máu và hệ tuần hoàn
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 32 Hệ hô hấp ở người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 33 Môi trường trong cơ thể và hệ bài tiết ở người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 34 Hệ thần kinh và các giác quan ở người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 35 Hệ nội tiết ở người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 36 Da và điều hoà thân nhiệt ở người
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 37 Sinh sản ở người
CHỦ ĐỀ 8: SINH THÁI
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 38 Môi trường và các nhân tố sinh thái
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 39 Quần thể sinh vật
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 40 Quần xã sinh vật
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 41 Hệ sinh thái
- Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 42 Cân bằng tự nhiên và bảo vệ môi trường
Giải bài tập sách bài tập (SBT) KHTN 8 cánh diều bài 6 Nồng độ dung dịch
https://s.shopee.vn/6Ai1QhN7jj
Hướng dẫn giải bài 6 Nồng độ dung dịch sách bài tập (SBT) KHTN 8 cánh diều trang 16
Bài tập này nằm trong sách "Cánh diều" được biên soạn theo chương trình đổi mới của Bộ giáo dục. Mục tiêu của bài tập là giúp học sinh làm quen với việc tính toán nồng độ dung dịch một cách chính xác và hiểu biết.
Để giải bài tập này, trước hết bạn cần xác định các thông số cần thiết như khối lượng và thể tích của dung dịch. Sau đó, áp dụng công thức tính nồng độ để tìm ra kết quả cuối cùng. Hãy lưu ý trong quá trình giải bài tập cần chú ý đến đơn vị đo lường và làm đúng từng bước một để tránh sai sót.
Qua việc thực hành giải bài tập này, hy vọng học sinh sẽ nắm vững kiến thức về nồng độ dung dịch và có thêm kỹ năng tính toán hiệu quả trong quá trình học tập.
Bài tập và hướng dẫn giải
Câu 6.1 Ở 25 °C, 250 gam nước có thể hoà tan tối đa 80 gam KNO3. Độ tan của KNO3 ở 25 °C
A. 32 gam/100 gam H2O. B. 36 gam/100 gam H2O.
C. 80 gam/100 gam H2O. D. 40 gam/100 gam H2O.
Câu 6.2 Khối lượng CuSO4 có trong 100 ml dung dịch CuSO4 0,5 M là
A. 80 gam. B. 160 gam. C. 16 gam. D. 8 gam.
Câu 6.3 Rót 300 ml nước vào bình có chứa sẵn 200 ml sodium chloride 0,50 M và lắc đều, thu được dung dịch sodium chloride mới. Nồng độ mol của dung dịch thu được là
A. 0,05 M. B. 0,10 M. C. 0,20 M. D. 0,30 M.
Câu 6.4 Đồ thị sau cho biết ảnh hưởng của nhiệt độ đến độ tan của ba chất khác nhau trong nước.
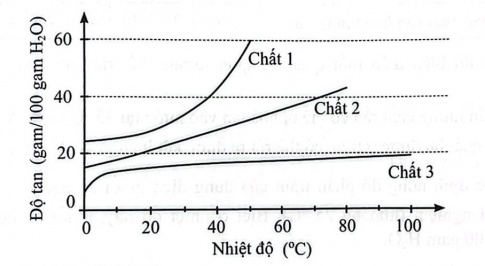
Nhận xét nào sau đây là đúng?
A. Đối với chất 1, khi nhiệt độ tăng thì độ tan giảm.
B. Độ tan của chất 2 ở 70 °C gấp đôi ở 0 °C.
C. Ở 20 °C, độ tan của chất 1 gần gấp đôi chất 3.
D. Độ tan của chất 3 ở 60 °C lớn hơn độ tan của chất 1 ở 20 °C.
Câu 6.5 Sử dụng từ ngữ thích hợp cho sẵn để điền vào chỗ ..... Mỗi từ ngữ có thể sử dụng một lần, nhiều hơn một lần hoặc không lần nào.
hoà tan bão hoà nước hỗn hợp nhiệt độ chất không tan
dung môi thể rắn chất tan bay hơi thể tích dung dịch
Dung dịch là ...(a)... lỏng đồng nhất của các chất đã tan trong nhau. Chất tan là chất ...(b)…. trong chất lỏng. Chất lỏng hoà tan chất tan được gọi là ...(c)... Chất tan và dung môi tạo thành ...(d)... Chất rắn không tan trong chất lỏng được gọi là ...(e)...
Độ tan của một chất rắn trong nước được đo bằng lượng chất rắn có trong 100 gam …(g)... Độ tan của một chất phụ thuộc vào ...(h)...
Câu 6.6 Đọc thông tin và lựa chọn số liệu thích hợp điền vào chỗ … trong các câu sau:
Cách pha chế 50 ml dung dịch NaOH nồng độ 1 M: cân ...(1)... gam NaOH, cho vào cốc thuỷ tinh dung tích 100 ml. Đổ dần nước cất vào cốc và khuấy nhẹ đến
...(2)... ml thì dừng lại, thu được ...(3)... ml dung dịch NaOH nồng độ ...(4)... M.
Câu 6.7 Để kiểm tra độ tan của một chất rắn chưa biết, một nhóm học sinh cho chất rắn đó vào 200 ml nước. Kết quả cho thấy độ tan của chất rắn thay đổi ở các nhiệt độ khác nhau của nước. Cụ thể như sau:
| Nhiệt độ của nước (°C) | 25 | 30 | 45 | 55 | 65 | 70 | 75 |
| Khối lượng chất rắn hoà tan (gam) | 17 | 20 | 32 | 40 | 46 | 49 | 52 |
a) Vẽ đồ thị biểu diễn mối quan hệ giữa lượng chất rắn hoà tan và nhiệt độ của nước.
b) Dự đoán lượng chất rắn có thể bị hoà tan vào nước tại 35 °C và 80 °C.
c) Từ kết quả thu được ở trên, có thể rút ra được kết luận gì về độ tan của chất?
Câu 6.8 Xác định nồng độ phần trăm của dung dịch muối ăn bão hoà ở nhiệt độ phòng thí nghiệm (khoảng 25 °C). Biết ở nhiệt độ này, muối ăn có độ tan là 36 gam/100 gam H2O.
Câu 6.9 Tính nồng độ mol của dung dịch sulfuric acid biết 250 ml dung dịch chứa 9,8 gam H2SO4.
Câu 6.10 Cần cho thêm bao nhiêu gam NaOH vào 120 gam dung dịch NaOH 20% để thu được dung dịch có nồng độ 25%?
Câu 6.11 25 ml sodium hydroxide 0,20 M phản ứng vừa đủ với 10 ml hydrochloric acid theo phương trình hoá học: HCl + NaOH → NaCl + H2O.
Xác định nồng độ mol của dung dịch acid.
Câu 6.12 Quan sát dụng cụ chứa dung dịch hydrochloric acid 0,01 M (hình 6.1).
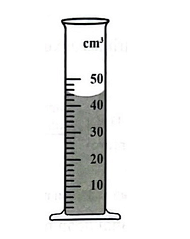
Hình 6.1
a) Cho biết tên của dụng cụ thí nghiệm.
b) Xác định thể tích của dung dịch hydrochloric acid.
c) Tính số mol của hydrochloric acid trong dụng cụ trên.
Câu 6.13 Từ dung dịch NaCl 1 M, hãy trình bày cách pha chế 250 ml dung dịch NaCl 0,2 M.
Giải bài tập sách giáo khoa (SGK) lớp 8 kết nối tri thức
- Soạn văn lớp 8 kết nối tri thức
- Soạn văn lớp 8 tập 1 kết nối tri thức
- Soạn văn lớp 8 tập 2 kết nối tri thức
- Giải bài tập toán lớp 8 kết nối tri thức
- Giải bài tập toán lớp 8 tập 1 kết nối tri thức
- Giải bài tập toán lớp 8 tập 2 kết nối tri thức
- Giải bài tập khoa học tự nhiên lớp 8 kết nối tri thức
- Giải bài tập hóa học lớp 8 kết nối tri thức
- Giải bài tập vật lí lớp 8 kết nối tri thức
- Giải bài tập sinh học lớp 8 kết nối tri thức
- Giải bài tập lịch sử và địa lí lớp 8 kết nối tri thức
- Giải bài tập công dân lớp 8 kết nối tri thức
- Giải bài tập công nghệ lớp 8 kết nối tri thức
- Giải bài tập tin học lớp 8 kết nối tri thức
- Giải bài tập mĩ thuật lớp 8 kết nối tri thức
- Giải bài tập âm nhạc lớp 8 kết nối tri thức
- Giải bài tập hoạt động trải nghiệm lớp 8 kết nối tri thức
Giải bài tập sách giáo khoa (SGK) lớp 8 chân trời sáng tạo
- Soạn văn lớp 8 chân trời sáng tạo
- Soạn văn lớp 8 tập 1 chân trời sáng tạo
- Soạn văn lớp 8 tập 2 chân trời sáng tạo
- Giải bài tập toán lớp 8 chân trời sáng tạo
- Giải bài tập toán lớp 8 tập 1 chân trời sáng tạo
- Giải bài tập toán lớp 8 tập 2 chân trời sáng tạo
- Giải bài tập lịch sử và địa lí lớp 8 chân trời sáng tạo
- Giải bài tập công dân lớp 8 chân trời sáng tạo
- Giải bài tập công nghệ lớp 8 chân trời sáng tạo
- Giải bài tập tin học lớp 8 chân trời sáng tạo
- Giải bài tập âm nhạc lớp 8 chân trời sáng tạo
- Giải bài tập mĩ thuật lớp 8 chân trời sáng tạo bản 1
- Giải bài tập mĩ thuật lớp 8 chân trời sáng tạo bản 2
- Giải bài tập hoạt động trải nghiệm lớp 8 chân trời sáng tạo bản 1
- Giải bài tập hoạt động trải nghiệm lớp 8 chân trời sáng tạo bản 2
Giải bài tập sách giáo khoa (SGK) lớp 8 cánh diều
- Soạn văn lớp 8 cánh diều
- Soạn văn lớp 8 tập 1 cánh diều
- Soạn văn lớp 8 tập 2 cánh diều
- Giải bài tập toán lớp 8 cánh diều
- Giải bài tập toán lớp 8 tập 1 cánh diều
- Giải bài tập toán lớp 8 tập 2 cánh diều
- Giải bài tập khoa học tự nhiên lớp 8 cánh diều
- Giải bài tập hóa học lớp 8 cánh diều
- Giải bài tập vật lí lớp 8 cánh diều
- Giải bài tập sinh học lớp 8 cánh diều
- Giải bài tập lịch sử và địa lí lớp 8 cánh diều
- Giải bài tập công dân lớp 8 cánh diều
- Giải bài tập công nghệ lớp 8 cánh diều
- Giải bài tập tin học lớp 8 cánh diều
- Giải bài tập mĩ thuật lớp 8 cánh diều
- Giải bài tập âm nhạc lớp 8 cánh diều
- Giải bài tập hoạt động trải nghiệm lớp 8 cánh diều
Giải bài tập sách bài tập (SBT) lớp 8 kết nối tri thức
- Soạn sách bài tập (SBT) ngữ văn lớp 8 kết nối tri thức
- Soạn sách bài tập (SBT) ngữ văn lớp 8 tập 1 kết nối tri thức
- Soạn sách bài tập (SBT) ngữ văn lớp 8 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 8 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 8 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) khoa học tự nhiên lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hóa học lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) vật lí lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) sinh học lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) lịch sử và địa lí lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) công dân lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) công nghệ lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tin học lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) âm nhạc lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) mĩ thuật lớp 8 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 8 kết nối tri thức
Giải bài tập sách bài tập (SBT) lớp 8 chân trời sáng tạo
- Soạn sách bài tập (SBT) ngữ văn lớp 8 tập 1 chân trời sáng tạo
- Soạn sách bài tập (SBT) ngữ văn lớp 8 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 8 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 8 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 8 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) lịch sử và địa lí lớp 8 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) công dân lớp 8 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) tin học lớp 8 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) công nghệ lớp 8 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) âm nhạc lớp 8 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) mĩ thuật lớp 8 chân trời sáng tạo bản 1
- Giải bài tập sách bài tập (SBT) mĩ thuật lớp 8 chân trời sáng tạo bản 2
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 8 chân trời sáng tạo bản 1
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 8 chân trời sáng tạo bản 2
Soạn sách bài tập (SBT) lớp 8 cánh diều
- Soạn sách bài tập (SBT) ngữ văn lớp 8 tập 1 cánh diều
- Soạn sách bài tập (SBT) ngữ văn lớp 8 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 8 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 8 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) khoa học tự nhiên lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) hóa học lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) vật lí lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) sinh học lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) lịch sử và địa lí lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) công dân lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) công nghệ lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) tin học lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) âm nhạc lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) mĩ thuật lớp 8 cánh diều
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 8 cánh diều




