Câu 6.12 Quan sát dụng cụ chứa dung dịch hydrochloric acid 0,01 M (hình 6.1).Hình 6.1a) Cho biết...
Câu hỏi:
Câu 6.12 Quan sát dụng cụ chứa dung dịch hydrochloric acid 0,01 M (hình 6.1).
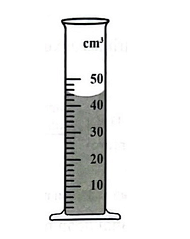
Hình 6.1
a) Cho biết tên của dụng cụ thí nghiệm.
b) Xác định thể tích của dung dịch hydrochloric acid.
c) Tính số mol của hydrochloric acid trong dụng cụ trên.
Câu trả lời:
Người trả lời: GV. Đỗ Văn Ngọc
Cách 1:a) Để xác định tên của dụng cụ thí nghiệm, chúng ta cần quan sát hình 6.1. Từ hình, chúng ta có thể nhận ra rằng dụng cụ được sử dụng là ống đong.b) Để xác định thể tích của dung dịch hydrochloric acid, ta chỉ cần đọc giá trị trên ống đong, đó là 44 ml (hoặc 44 cm$^{3}$).c) Để tính số mol của hydrochloric acid trong dụng cụ trên, ta sử dụng công thức: số mol = thể tích dung dịch (l) x nồng độ mol/lit. Nếu thể tích dung dịch là 44 ml, có nồng độ 0,01 M thì số mol của hydrochloric acid là: 0,044 x 0,01 = 4,4 x $10^{-4}$ mol.Cách 2:a) Dụng cụ thí nghiệm được sử dụng trong trường hợp này là ống đong.b) Thể tích của dung dịch hydrochloric acid được cho trên ống đong là 44 ml hay 44 cm$^{3}$.c) Để tính số mol của hydrochloric acid trong dụng cụ, ta sử dụng công thức: số mol = thể tích dung dịch (lit) x nồng độ mol/lit. Với thể tích dung dịch là 44 ml và nồng độ 0,01 M, ta có: 0,044 x 0,01 = 4,4 x $10^{-4}$ mol.Câu trả lời chi tiết và đầy đủ:a) Tên của dụng cụ thí nghiệm là ống đong.b) Thể tích của dung dịch hydrochloric acid là 44 ml (hoặc 44 cm$^{3}$).c) Số mol của hydrochloric acid trong dụng cụ trên là 4,4 x $10^{-4}$ mol.
Câu hỏi liên quan:
- Câu 6.1 Ở 25 °C, 250 gam nước có thể hoà tan tối đa 80 gam KNO3. Độ tan của KNO3 ở25 °CA. 32...
- Câu 6.2 Khối lượng CuSO4 có trong 100 ml dung dịch CuSO4 0,5 M làA. 80 gam. ...
- Câu 6.3 Rót 300 ml nước vào bình có chứa sẵn 200 ml sodium chloride 0,50 M và lắc đều, thu được...
- Câu 6.4 Đồ thị sau cho biết ảnh hưởng của nhiệt độ đến độ tan của ba chất khác nhau trong nước.Nhận...
- Câu 6.5 Sử dụng từ ngữ thích hợp cho sẵn để điền vào chỗ ..... Mỗi từ ngữ có thể sử dụng một lần,...
- Câu 6.6 Đọc thông tin và lựa chọn số liệu thích hợp điền vào chỗ … trong các câu sau:Cách pha chế 5...
- Câu 6.7 Để kiểm tra độ tan của một chất rắn chưa biết, một nhóm học sinh cho chất rắn đó vào 200 ml...
- Câu 6.8 Xác định nồng độ phần trăm của dung dịch muối ăn bão hoà ở nhiệt độ phòng thí nghiệm...
- Câu 6.9 Tính nồng độ mol của dung dịch sulfuric acid biết 250 ml dung dịch chứa 9,8 gam H2SO4.
- Câu 6.10 Cần cho thêm bao nhiêu gam NaOH vào 120 gam dung dịch NaOH 20% để thu được dung dịch có...
- Câu 6.11 25 ml sodium hydroxide 0,20 M phản ứng vừa đủ với 10 ml hydrochloric acid theo phương...
- Câu 6.13 Từ dung dịch NaCl 1 M, hãy trình bày cách pha chế 250 ml dung dịch NaCl 0,2 M.





Vui lòng cung cấp thêm thông tin để có thể tính toán chính xác số mol của hydrochloric acid trong dụng cụ.
c) Để tính số mol của hydrochloric acid trong dụng cụ trên, ta cần biết thể tích của dung dịch hydrochloric acid và sử dụng công thức số mol = nồng độ x thể tích (mol = M x V).
b) Thể tích của dung dịch hydrochloric acid được đưa vào không được nêu rõ trong đề bài, nên không thể xác định được.
a) Dụng cụ thí nghiệm trong hình 6.1 là bình đựng dung dịch hydrochloric acid.