CHỦ ĐỀ 1: NGUYÊN TỬ. NGUYÊN TỐ HÓA HỌC
CHỦ ĐỀ 2" SƠ LƯỢC VỀ BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
CHỦ ĐỀ 3: PHÂN TỬ
CHỦ ĐỀ 4: TỐC ĐỘ
CHỦ ĐỀ 5: ÂM THANH
CHỦ ĐỀ 6: ÁNH SÁNG
CHỦ ĐỀ 7: TÍNH CHẤT TỪ CỦA CHẤT
CHỦ ĐỀ 8: TRAO ĐỔI CHẤT VÀ CHUYỂN HÓA NĂNG LƯỢNG Ở SINH VẬT
- Giải bài tập 17 Vai trò của trao đổi chất và chuyển hóa năng lượng ở sinh vật
- Giải bài tập 18 Quang hợp ở thực vật
- Giải bài tập 19 Các yếu tố ảnh hưởng đến quang hợp
- Giải bài tập 21 Hô hấp tế bào
- Giải bài tập 22 Các yếu tố ảnh hưởng đến hô hấp tế bào
- Giải bài tập 23 Trao đổi khí ở sinh vật
- Giải bài tập 24 Vai trò của nước và các chất dinh dưỡng đối với cơ thể sinh vật
- Giải bài tập 25 Trao đổi nước và các chất dinh dưỡng ở thực vật
- Giải bài tập 26 Trao đổi nước và các chất dinh dưỡng ở động vật
- Giải bài tập Bài tập chủ đề 8
CHỦ ĐỀ 9: CẢM ỨNG Ở SINH VẬT
CHỦ ĐỀ 10: SINH TRƯỞNG VÀ PHÁT TRIỂN Ở SINH VẬT
CHỦ ĐỀ 11: SINH SẢN Ở SINH VẬT
CHỦ ĐỀ 12: CƠ THỂ SINH VẬT LÀ MỘT THỂ THỐNG NHẤT
Giải bài tập 5 Giới thiệu về liên kết hóa học
https://s.shopee.vn/6Ai1QhN7jj
Giải bài tập 5: Giới thiệu về liên kết hóa học - sách cánh diều khoa học tự nhiên 7
Trong phần này, chúng ta sẽ tìm hiểu về liên kết hóa học qua các bài tập trong sách giáo khoa. Việc nắm vững kiến thức bài học sẽ giúp các em học sinh hiểu rõ hơn về cấu trúc và tính chất của các phân tử và ion.
I. Đặc điểm cấu tạo vỏ nguyên tử khí hiếm
Câu hỏi 1: Quan sát hình 5.1, hãy cho biết số electron ở lớp ngoài cùng của vỏ nguyên tử khí hiếm.
Hướng dẫn giải: Lớp ngoài cùng của vỏ nguyên tử khí hiếm thường chứa 8 electron, trừ nguyên tố Helium (He) chỉ chứa 2 electron.
II. Liên kết ion
1. Sự tạo thành liên kết trong phân tử sodium chloride
Câu hỏi 2: Quan sát hình 5.2 và 5.3, cho biết lớp vỏ của các ion $Na^+$, $Cl^-$ tương tự vỏ nguyên tử của nguyên tố khí hiếm nào?
Hướng dẫn giải: Ion $Na^+$ có lớp vỏ tương tự với Ne, trong khi ion $Cl^-$ có lớp vỏ giống với Ar.
Câu hỏi 3: Quan sát hình 5.2, hãy so sánh về số electron, số lớp electron giữa nguyên tử Na và Na+
Hướng dẫn giải: Nguyên tử Na có 11 electron và 3 lớp electron, trong khi ion Na+ chỉ có 10 electron và 2 lớp electron sau khi mất 1 electron.
Luyện tập 1: Khi nguyên tử K liên kết với F để tạo phân tử potassium fluoride, nguyên tử K sẽ nhận 1 electron để đạt cấu hình electron bền vững của khí hiếm. Sơ đồ tạo liên kết trong phân tử potassium fluoride có thể được vẽ ra để minh họa quá trình này.
Để hiểu rõ hơn về liên kết hóa học, các em hãy thực hành bài tập và luyện tập để củng cố kiến thức và kỹ năng của mình.
Bài tập và hướng dẫn giải
2. Sự tạo thành liên kết trong phân tử magnesium oxide
Câu hỏi 4. Quan sát hình 5.5 và 5.6 và cho biết các ion Mg2+ và O2- có lớp vỏ tương đương khí hiếm nào?
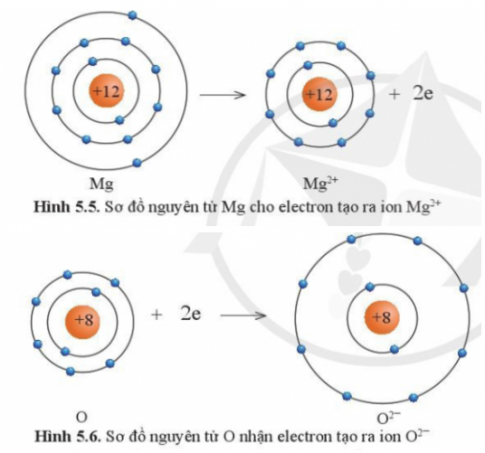
Câu hỏi 5. Quan sát hình 5.5 hãy so sánh về số electron, số lớp electron giữa nguyên tử Mg và ion Mg2+
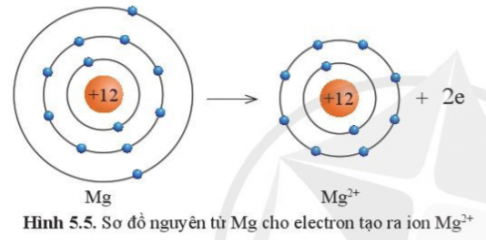
Luyện tập 2. Nguyên tử Ca có 2 electron ở lớp ngoài cùng. Hãy vẽ sơ đồ tạo thành liên kết khi nguyên tử Ca kết hợp với nguyên tử O tạo ra phân tử calcium oxide
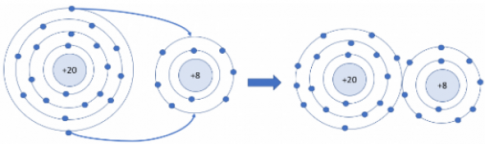
Luyện tập 3. Nguyên tử K kết hợp với nguyên tử Cl tạo thành phân tử potassium chloride. Theo em, ở điều kiện thường, potassium chloride là chất rắn, chất lỏng hay chất khí? Vì sao?
III. Liên kết cộng hoá trị
1. Sự tạo thành liên kết trong phân tử hydrogen
Câu hỏi 6. Quan sát hình 5.9 , hãy cho biết nguyên tử H trong phân tử Hydrogen có lớp vỏ tương tự khí hiếm nào?
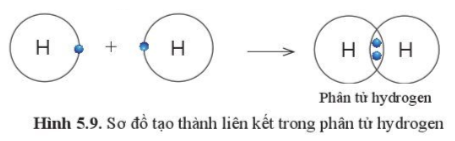
Luyện tập 4. Hai nguyên tử Cl liên kết với nhau tạo thành phân tử chlorine
a) Mỗi nguyên tử Cl cần thêm bao nhiêu electron vào lớp ngoài cùng để có lớp vỏ tương tự khí hiếm
b) Hãy vẽ sơ đồ tạo thành liên kết trong phân tử chlorine
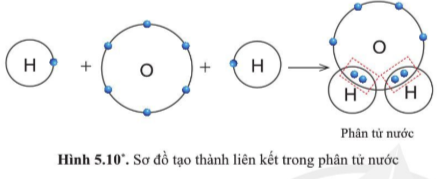
2. Sự tạo thành liên kết trong phân tử nước
Câu hỏi 7. Quan sát hình 5.10, trong phân tử nước, mỗi nguyên tử H và O có bao nhiêu electron ở lớp ngoài cùng
Luyện tập 5. Mỗi nguyên tử H kết hợp với 1 nguyên tử Cl tạo thành phân tử hydrogen chloride. Hãy vẽ sơ đồ tạo thành phân tử hydrogen chloride từ nguyên tử H và nguyên tử Cl
Luyện tập 6. Mỗi nguyên tử N kết hợp với 3 nguyên tử H tạo thành phân tử ammonia. Hãy vẽ sơ đồ tạo thành liên kết trong phân tử ammonia.
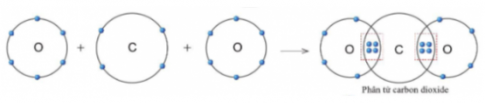
3. Sự tạo thành liên kết trong phân tử carbon dioxide
Câu hỏi 8. Quan sát hình 5.11, hãy cho biết trong phân tử khí carbon dioxide, nguyên tử cacbon có bao nhiêu electron dùng chung với nguyên tử O
Luyện tập 7. Hai nguyên tử N kết hợp với nhau tạo thành phân tử nitrogen. Hãy vẽ sơ đồ tạo thành liên kết trong phân tử nitrogen
Vận dụng. Hãy giải thích các hiện tượng sau:
a) Nước tinh khiết hầu như không dẫn điện, nhưng nước biển lại dẫn được điện.
b) Khi cho đường ăn vào chảo rồi đun nóng sẽ thấy đường ăn nhanh chóng chuyển từ thể rắn sang thể lỏng, làm như vậy với muối ăn thấy muối ăn vẫn ở thể rắn
Câu hỏi 9. So sánh một số tính chất chung của chất cộng hoá trị với chất ion
Giải bài tập sách giáo khoa (SGK) lớp 7 kết nối tri thức
- Giải bài tập toán lớp 7 tập 1 kết nối tri thức
- Giải bài tập toán lớp 7 tập 2 kết nối tri thức
- Soạn văn lớp 7 tập 1 kết nối tri thức
- Soạn văn lớp 7 tập 2 kết nối tri thức
- Văn mẫu lớp 7 kết nối tri thức
- Giải bài tập khoa học tự nhiên lớp 7 kết nối tri thức
- Giải bài tập vật lí lớp 7 kết nối tri thức
- Giải bài tập hóa học lớp 7 kết nối tri thức
- Giải bài tập sinh học lớp 7 kết nối tri thức
- Giải bài tập lịch sử và địa lí lớp 7 kết nối tri thức
- Giải bài tập lịch sử lớp 7 kết nối tri thức
- Giải bài tập địa lí lớp 7 kết nối tri thức
- Giải bài tập hoạt động trải nghiệm lớp 7 kết nối tri thức
- Giải bài tập mĩ thuật lớp 7 kết nối tri thức
- Giải bài tập âm nhạc lớp 7 kết nối tri thức
- Giải bài tập công dân lớp 7 kết nối tri thức
- Giải bài tập công nghệ lớp 7 kết nối tri thức
- Giải bài tập tin học lớp 7 kết nối tri thức
- Giải bài tập giáo dục thể chất lớp 7 kết nối tri thức
Giải bài tập sách giáo khoa (SGK) lớp 7 chân trời sáng tạo
- Giải bài tập toán lớp 7 tập 1 chân trời sáng tạo
- Giải bài tập toán lớp 7 tập 2 chân trời sáng tạo
- Soạn văn lớp 7 tập 1 chân trời sáng tạo
- Soạn văn lớp 7 tập 2 chân trời sáng tạo
- Văn mẫu lớp 7 chân trời sáng tạo
- Giải bài tập khoa học tự nhiên lớp 7 chân trời sáng tạo
- Giải bài tập vật lí lớp 7 chân trời sáng tạo
- Giải bài tập hóa học lớp 7 chân trời sáng tạo
- Giải bài tập sinh học lớp 7 chân trời sáng tạo
- Giải bài tập lịch sử và địa lí lớp 7 chân trời sáng tạo
- Giải bài tập lịch sử lớp 7 chân trời sáng tạo
- Giải bài tập địa lí lớp 7 chân trời sáng tạo
- Giải bài tập hoạt động trải nghiệm lớp 7 chân trời sáng tạo
- Giải bài tập âm nhạc lớp 7 chân trời sáng tạo
- Giải bài tập mĩ thuật lớp 7 chân trời sáng tạo
- Giải bài tập công dân lớp 7 chân trời sáng tạo
- Giải bài tập tin học lớp 7 chân trời sáng tạo
- Giải bài tập công nghệ lớp 7 chân trời sáng tạo
- Giải bài tập giáo dục thể chất lớp 7 chân trời sáng tạo
Giải bài tập sách giáo khoa (SGK) lớp 7 cánh diều
- Giải bài tập toán lớp 7 tập 1 cánh diều
- Giải bài tập toán lớp 7 tập 2 cánh diều
- Soạn văn lớp 7 tập 1 cánh diều
- Soạn văn lớp 7 tập 2 cánh diều
- Văn mẫu lớp 7 cánh diều
- Giải bài tập khoa học tự nhiên lớp 7 cánh diều
- Giải bài tập vật lí lớp 7 cánh diều
- Giải bài tập hóa học lớp 7 cánh diều
- Giải bài tập sinh học lớp 7 cánh diều
- Giải bài tập lịch sử và địa lí lớp 7 cánh diều
- Giải bài tập lịch sử lớp 7 cánh diều
- Giải bài tập địa lí lớp 7 cánh diều
- Giải bài tập hoạt động trải nghiệm lớp 7 cánh diều
- Giải bài tập âm nhạc lớp 7 cánh diều
- Giải bài tập mĩ thuật lớp 7 cánh diều
- Giải bài tập tin học lớp 7 cánh diều
- Giải bài tập công dân lớp 7 cánh diều
- Giải bài tập công nghệ lớp 7 cánh diều
- Giải bài tập giáo dục thể chất lớp 7 cánh diều
Giải bài tập sách bài tập (SBT) lớp 7 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 7 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 7 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 7 tập 1 kết nối tri thức
- Giải bài tập sách bài tập (SBT) toán lớp 7 tập 2 kết nối tri thức
- Giải bài tập sách bài tập (SBT) khoa học tự nhiên lớp 7 kết nối tri thức
- Giải bài tập sách bài tập (SBT) lịch sử và địa lí lớp 7 kết nối tri thức
- Giải bài tập sách bài tập (SBT) công nghệ lớp 7 kết nối tri thức
- Giải bài tập sách bài tập (SBT) tin học lớp 7 kết nối tri thức
- Giải bài tập sách bài tập (SBT) công dân lớp 7 kết nối tri thức
- Giải bài tập sách bài tập (SBT) mĩ thuật lớp 7 kết nối tri thức
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 7 kết nối tri thức
Giải bài tập sách bài tập (SBT) lớp 7 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 7 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) ngữ văn lớp 7 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 7 tập 1 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) toán lớp 7 tập 2 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) khoa học tự nhiên lớp 7 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) lịch sử và địa lí lớp 7 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) công nghệ lớp 7 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) tin học lớp 7 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) công dân lớp 7 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) mĩ thuật lớp 7 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) âm nhạc lớp 7 chân trời sáng tạo
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 7 chân trời sáng tạo bản 1
- Giải bài tập sách bài tập (SBT) hoạt động trải nghiệm lớp 7 chân trời sáng tạo bản 2
Giải bài tập sách bài tập (SBT) lớp 7 cánh diều
- Giải bài tập sách bài tập (SBT) Ngữ văn lớp 7 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) Ngữ văn lớp 7 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 7 tập 1 cánh diều
- Giải bài tập sách bài tập (SBT) toán lớp 7 tập 2 cánh diều
- Giải bài tập sách bài tập (SBT) Khoa học tự nhiên lớp 7 cánh diều
- Giải bài tập sách bài tập (SBT) Lịch sử và địa lí lớp 7 cánh diều
- Giải bài tập sách bài tập (SBT) tin học lớp 7 cánh diều
- Giải bài tập sách bài tập (SBT) công dân lớp 7 cánh diều
- Giải bài tập sách bài tập (SBT) công nghệ lớp 7 cánh diều
- Giải bài tập sách bài tập (SBT) âm nhạc lớp 7 cánh diều
- Giải bài tập sách bài tập (SBT) Hoạt động trải nghiệm lớp 7 cánh diều




